Большая Советская
Энциклопедия
|
|
|
|
источник статьи: Большая Советская Энциклопедия |
|
Карбоновые кислоты, класс органических соединений, содержащих карбоксильную группу (карбоксил) Большинство К. к. имеет тривиальные названия, многие из которых связаны с их нахождением в природе, например муравьиная, яблочная, валериановая, лимонная кислоты. По Женевской номенклатуре наименования К. к. производят от названий углеводородов с тем же числом атомов углерода, прибавляя окончание «овая» и слово «кислота», например метанова я кислота (муравьиная), этановая кислота (уксусная) и т.д. Нередко К. к. рассматривают как производные углеводородов; например, кислоту строения HC º С — COOH называют ацетиленкарбоновой кислотой. Кислотные свойства обусловлены способностью К. к. к диссоциации в водном растворе: RCOOH Û RCOO- + H+. Как правило, К. к. слабее минеральных. Константы диссоциации одноосновных насыщенных кислот жирного ряда при 25°С изменяются от 1,7×10-4 (муравьиная кислота) до 1,3.10-5 (высшие гомологи). Сила К. к. существенно зависит также от электрофильности радикала, связанного с карбоксилом. Введение электроотрицательных заместителей (например, NO2, CN, Cl) в положение, соседнее с карбоксильной группой, резко повышает кислотность, например циануксусная кислота CNCH К. к. — жидкие (например, низшие жирные кислоты) или твёрдые (например, высшие жирные и ароматичес кие кислоты) вещества (см. табл.). Низшие члены насыщенных К. к. жирного ряда хорошо растворимы в воде, средние члены (C4 — C10), а также ароматические кислоты — ограниченно, высшие жирные кислоты в воде не растворимы; как и ароматические кислоты, они хорошо растворяются в спирте, эфире, бензоле. Наиболее важные химические свойства К. к. — способность превращаться в производные. При взаимодействии с основаниями К. к. дают соли: RCOOH + NaOH ® RCOONa + H2O. При действии на К. к. спиртов в присутствии минеральных кислот легко образуются эфиры сложные: RCOOH + R'OH ® RCOOR' + H2O; при действии галогенангидридов минеральных кислот (например, PCl3, POCl3, SOCl2)— галогенангидриды К. к. RCOX (X — атом галогена). При нагревании кислот с водоотнимающими средствами получаются ангидриды К. к. (RCO)2O. Галогенангидриды и ангидриды К. к. применяют как ацилирующие агенты. Отщепление воды от аммониевых солей К. к. (1) и реакция галогенангидридов с аммиаком (2) приводят к амидам кислот: 1) RCOONH4 ® RCONH2 + H2O 2) RCOCI + 2NH3 ® RCONH2 + NH4CI. Методы получения К. к. весьма многочисленны. Окислением первичных спиртов и альдегидов получают К. к. с тем же числом атомов углерода. Окисление кетонов сопровождается разрывом связи С—С; из циклических кетонов образуются дикарбоновые кислоты, например адипиновая кислота из циклогексанона: < p>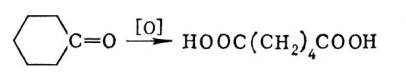 Насыщенные углеводороды могут быть подвергнуты деструктивному окислению с образованием смеси продуктов, в том числе и карбоновых кислот. Этим методом из 1 m парафина обычно получают около 350 кг К. к. Окисление боковой цепи жирно-ароматических углеводородов либо многоядерных ароматических углеводородов приводит к ароматическим К. к.; например, фталевая кислота получается окислением о-ксилола или нафталина:
Ненасыщенные углеводороды окисляются по месту двойной связи:
Важный метод синтеза К. к. — гидролиз их нитрилов, легко получаемых взаимодействием галогенопроизводных углеводородов с цианистым натрием: RCI + NaCN ® RCN ® RCOOH. В настоящее время промышленное значение приоб рёл метод синтеза К. к. карбонилированием, т. е. введением группы CO в органические соединения:
Некоторые К. к. получают из природных продуктов. Так, щелочным гидролизом (омылением) жиров получают соли высших жирных кислот (мыла) и глицерин. Лимонную кислоту получают из ботвы хлопчатника и из стеблей махорки (после выделения из них никотина). Многие К. к. получают сбраживанием углеводов в присутствии бактерий определённого вида (маслянокислое, молочнокислое, лимоннокислое и др. виды брожения). К. к. широко распространены в природе в свободном состоянии и в виде производных (главным образом сложных эфиров). Так, в летучем масле герани содержится пеларгоновая кислота, в лимонах — лимонная. В состав животных и растительных жиров и масел входят глицериды высших нормальных К. к. жирного ряда, из которых преобладают пальмитиновая кислота, стеариновая кислота и олеиновая кислота. К. к., их производные, а также многочисленные соединения, содержащие наряду с карбоксильной иные функциональные группы (например, аминокислоты, оксикислоты и др.), имеют большое биологическое значение и находят разнообразное практическое применение. Муравьиную и уксусную кислоты, например, применяют при крашении и печатании тканей; уксусную кислоту и уксусный ангидрид — в производстве ацетилцеллюлозы. Аминокислоты входят в состав белко в. В медицине используют салициловую кислоту, n-аминосалициловую кислоту (ПАСК) и др. Высшие жирные К. к. широко применяют как сырьё для производства мыла, лаков и красок, поверхностно-активных веществ, как эмульгаторы в производстве каучуков, как пластификаторы в производстве резин и др. Адипиновая кислота — один из исходных продуктов в производстве полиамидного волокна (найлона), терефталевая — в производстве полиэфирного волокна (лавсана, терилена), полимерный нитрил акриловой кислоты (орлон) применяют как синтетическое волокно, близкое по свойствам к натуральной шерсти. Полимеры и сополимеры эфиров метакриловой кислоты используют как органическое стекло. Некоторые представители карбоновых кислот и их свойства
*В скобках указана температура (в °С). ** 1 мм рт. ст. = 133,322 н/м2.
Лит.: Неницеску К. Д., Органическая химия, пер. с рум., т. 1—2, М., 1962—1963; Несмеянов А. Н., Несмеянов Н. А., Начала органической химии, кн. 1—2, М., 1969—70. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||