Янтарная кислота и ее гомологи
— представляют предельные двухосновные кислоты общей формулы С n Н 2n (СО 2 Н) 2
= С m Н 2m-2
О 4, заключающие в
молекуле группу атомов —
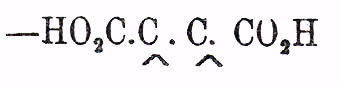 , свободные
сродства которой насыщены водородом (Я. кислота) или более или менее сложными
одноатомными остатками общей формулы (С nH2n+1)'
[гомологи Я. кислоты]. Вполне резких признаков, позволяющих установить
наличность указанной группировки в данной двуосновной предельной кислоте, не
имеется, и потому о присутствии ее судят главным образом на основании
синтетических реакций образования кислоты. Гомологи Я. кислоты отличаются от
замещенных малоновых кислот неспособностью распадаться при температуре плавления
(и несколько выше) на углекислый газ и одноосновную предельную кислоту. От
кислот глутаровых и некоторых других изомерных кислот они отличаются тем, что
при перегонке распадаются на воду и ангидрид: С n Н 2n (СО 2 Н) 2
= H2 O + С nH2n(C2O3);
последний в бензольном (хлороформенном, эфирном) растворе образует с анилином
(п. толуидином, β-нафтиламином) труднорастворимую аниловую кис. , свободные
сродства которой насыщены водородом (Я. кислота) или более или менее сложными
одноатомными остатками общей формулы (С nH2n+1)'
[гомологи Я. кислоты]. Вполне резких признаков, позволяющих установить
наличность указанной группировки в данной двуосновной предельной кислоте, не
имеется, и потому о присутствии ее судят главным образом на основании
синтетических реакций образования кислоты. Гомологи Я. кислоты отличаются от
замещенных малоновых кислот неспособностью распадаться при температуре плавления
(и несколько выше) на углекислый газ и одноосновную предельную кислоту. От
кислот глутаровых и некоторых других изомерных кислот они отличаются тем, что
при перегонке распадаются на воду и ангидрид: С n Н 2n (СО 2 Н) 2
= H2 O + С nH2n(C2O3);
последний в бензольном (хлороформенном, эфирном) растворе образует с анилином
(п. толуидином, β-нафтиламином) труднорастворимую аниловую кис.
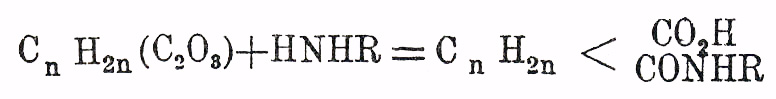
(Anschü tz), переходящую при
кратковременном нагревании выше температуры плавления (Auwers), или при
водоотнимающем действии хлористого ацетила (фосфорного ангидрида, Ansch ü tz),
с потерей воды в анил
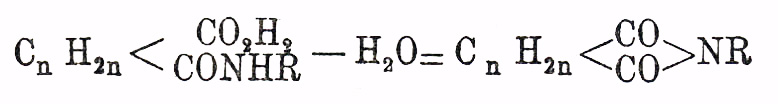
(Anschü tz, Auwers, "L. A.", 261
и 285); глутаровые кислоты большей частью способны перегоняться без разложения и
их аниловые кислоты не теряют воды при нагревании; впрочем, как было уже
замечено, резкого, качественного различия между реакциями этих изомеров (кислот
янтарных и глутаровых) установить невозможно. Реакциями образования Я. кислот
признаются: 1) окисление соответственных двупервичных гликолей (см.)
[соответственных оксиальдегидов, диальдегидов, первичных спиртокислот,
альдегидо-кислот): (НО)Н 2 С.СН 2.СН 2 СН 2 (ОН)
+ 40" = (НО)ОС.СН 2.СН 2.СО(ОН)+2Н 2 О;
2) гидрогенизация непредельных двуосновных кисл. общей формулы С nH2n-4O4
(см. кислоты: малеиновую, фумаровую, цитраконовую): НО 2 С.СН:СН.СО 2 Н
+ H 2 = НО 2 С.СН 2.СH 2.СО 2 Н;
3) восстановление (гидрогенизация) соответственных окси-(диокси), или
галоидозамещенных двуосновных предельных кислот: НО 2 С.СН(ОН).СН(ОН).СО 2 Н
(винная кислота, см.) + 4HJ = НО 2 С.СН 2.СН 2 СО 2 Н
+ 2Н 2 О + 2J 2,
НО 2 С.СH(ОН).СН 2.СО 2 Н
(яблочная кислота, см.) + 2HJ = НО 2 С.СН 2.СH 2,.
CO2H + H2O + J2
и HO 2C.CHCl.CH2 COH
(хлороянтарная кисл.) +Н 2
= НО 2 C.СН 2.СH 2 СО 2 Н
+ HCl; 4) действие молекулярного серебра (Wislicenus) или ртути (Vandevelde) на
моногалоидо (хлоро, но преимущественно бромо-, йодо-) замещенные эфиры
предельных одноосновных кислот: H 5C2O2C.CH2 Cl
(монохлороуксусный эфир) + Hg + ClCH 2.CO2C2H5
= HgCl2 + Н 5 С 2O2 С.СН 2.СН 2.СО 2 С 2 Н 5
(эфир Я. кислоты); эта реакция
наименее чистая и часто ведет к образованию изомерных кисл. Я. и глутаровых;
напр. 2Н 5 С 2 О 2 С.СВr(СН 3)2
(бромизомасляный эфир) + 2Ag
= Н 5 С 2 О 2 С.СН(СН 3).СН 2.С(СН 3)2.СО 2 С 2 Н 5
(триметилглутаровый эфир) +
2AgBr; 5) действие KCN на моногалоидозамещенные предельные одноосновные кислоты
и омыление полученных нитрилов: Н 5 С 2O2 С.СH 2.СН 2 Х
(Х = Cl, Вr, J) + KCN=H 5C2O2C.CH2.CH2.CN
+ КХ и H 5C2O2 C.CН 2 СН 2.CN
+ 3H2 O = НО 2 С.СH 2 СН 2.СО 2 Н
+ С 2 Н 5 (ОН)
+ NH 3; реакция
может быть значительно усложнена, так как некоторые цианоэфиры способны замещать
водород (один, два атома) металлом (натрием напр.), который может быть, при
действии галоидалкилов (C 2H5 J
— йодистого этила, напр.) замещен эквивалентным числом одноатомных предельных
остатков (С N Н 2n+1)
(ср. ниже); 6) омыление соответственных двунитрилов, получаемых в свою очередь
при взаимодействии KCN (в спиртовом растворе) с двугалоидоэтиленами (двухлоро- и
двубромоэтиленами), т. е. такими двугалоидозамещенными парафинами — С N Н 2N Х 2
—, у которых оба атома галоида (X) находятся у соседних атомов углерода (ср.
Этилен, строение):
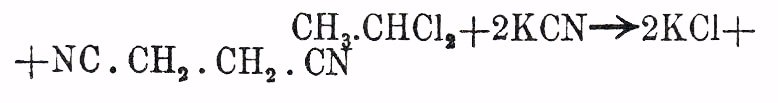 (двунитрил Я.
кислоты) и NC.CН 2.CH2.CN
+ 4Н 2 О = 2NH 3
+ НО 2 С.СН 2.СН 2.СО 2 Н;
и эта реакция, надо думать, не протекает без перегруппировок; так напр. только
что указанный двунитрил может быть получен при действии KCN на хлористый
этилиден: CH 3.CHCl2
+ 2KCN?2KCl + NC.СН 2.СH 2.CN,
т. е. на такое производное, у которого атомы галоида находятся у одного атома
углерода (Simpson, Erlenmeyer; ср. Этилен, строение); действие KCN на гомологи
хлористого этилидена не изучено систематически; 7) действие
α-моногалоидозамещенных эфиров предельных одноосновных кислот на
мононатрзамещенные малоновые эфиры, сопровождаемое омылением полученных эфиров и
разрушением нагреванием трикарбоновых кислот (см. Трикарболовые и
Четырехосновные кисл.): (двунитрил Я.
кислоты) и NC.CН 2.CH2.CN
+ 4Н 2 О = 2NH 3
+ НО 2 С.СН 2.СН 2.СО 2 Н;
и эта реакция, надо думать, не протекает без перегруппировок; так напр. только
что указанный двунитрил может быть получен при действии KCN на хлористый
этилиден: CH 3.CHCl2
+ 2KCN?2KCl + NC.СН 2.СH 2.CN,
т. е. на такое производное, у которого атомы галоида находятся у одного атома
углерода (Simpson, Erlenmeyer; ср. Этилен, строение); действие KCN на гомологи
хлористого этилидена не изучено систематически; 7) действие
α-моногалоидозамещенных эфиров предельных одноосновных кислот на
мононатрзамещенные малоновые эфиры, сопровождаемое омылением полученных эфиров и
разрушением нагреванием трикарбоновых кислот (см. Трикарболовые и
Четырехосновные кисл.):
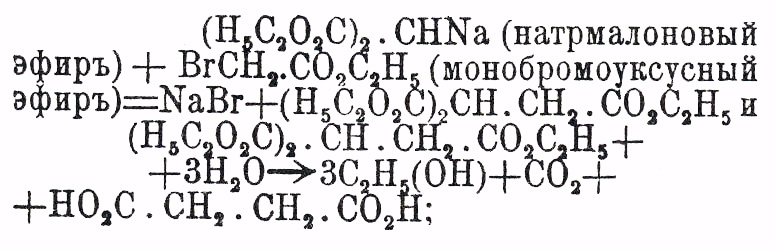
8) разрушение нагреванием соответственных трикарбоновых кислот (l. с.) или
четырехосновных (двумалоновых) кислот:
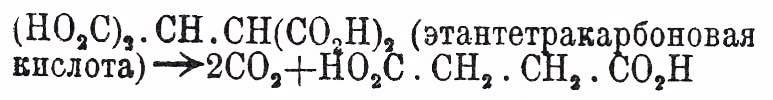 0действие
едких щелочей на продукты взаимодействия натрацетоуксусного эфира с α
моногалоидозамещенными эфирами предельных одноосновных кислот: 0действие
едких щелочей на продукты взаимодействия натрацетоуксусного эфира с α
моногалоидозамещенными эфирами предельных одноосновных кислот:
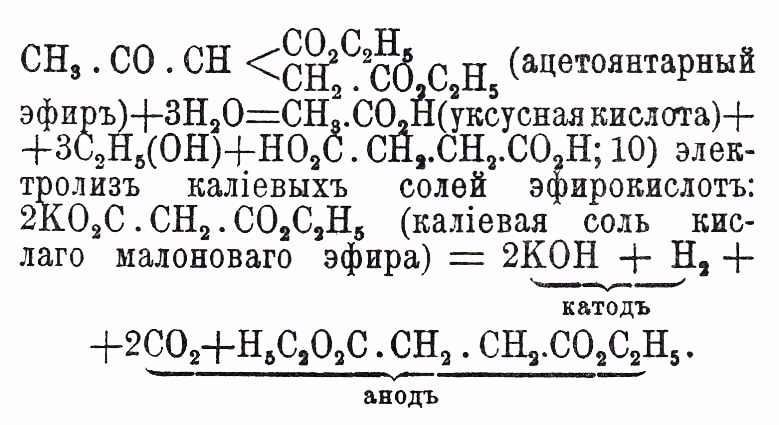
Между реакциями образования Я. кислоты и ее гомологов необходимо упомянуть
реакции окисления различных органических веществ; так напр. Я. кислота
образуется при окислении (преимущественно азотной кислотой): бутиролактона (см.)
и жиров (высших жирных кислот, см.); кислота изопропилянтарная —
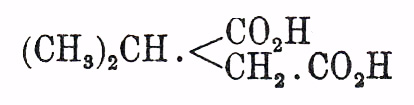
получена при окислении (марганцевокалиевой солью) тетрагидрокарбона (см.) и
т. п.; реакции эти не систематизированы и потому являются пока единичными; к
единичным же случаям образования относится и появление напр. Я. кислоты при
некоторых реакциях брожения (см. ниже). Число известных в настоящее время Я.
кислот и их производных громадно: достаточно для пояснения этого обстоятельства
заметить, например, что уже любая однозамещенная Я. кислота общей формулы HO 2C. СНR,.
СH 2.CO2 H
(где R=C NH2N+1),
содержа один асимметричный атом углерода, напечатанный курсивом, возможна уже в
трех формах: двух оптически деятельных (право- и левовращающих, см. Винная
кислота, Молочная кислота, Стереоизомерия, Стереохимия) и их рацемическом (и
псевдорацемических (?), см.) полимере; в симметрично двузамещенных Я. кисл.
общей формулы НО 2 С.СНХ.СНУ.СО 2 Н
имеются два асимметричных атома углерода (напечатаны курсивом), а потому число
возможных форм еще больше, усложняясь при тождестве Х и Y (X и Y одноатомные
остатки предельных углеводородов) появлением кислот мезо (анти; ср. Винная
кислота) типа. Впрочем, далеко не все теоретически возможные формы известны в
настоящее время. О номенклатуре Я. кислот см. соотв. ст. В настоящей статье
приходится ограничиться более подробным описанием самой Я. кислоты и указанием
некоторых наиболее замечательных реакций образования ее гомологов и некоторыми
свойствами последних. Я.
кислота — НО 2 С.CH 2.СН 2.СО 2 Н
= С 4 Н 6 О 4
известна еще Агриколе, как находящаяся в янтаре (Berzelius, Liebig и W ö hler,
D'Arcet); она встречается в скипидаре различного происхождения, в соке чистотела
(Chelidonium majus; Wolz, Zwenger), чечевицы (K ö hnke),
мака (Papaver somniferum), неспелого винограда (Bremmer, Brandenburg), свеклы
(v. Lippmann), ревеня (Brunner); в животных организмах она найдена в зобной
железе теленка, в щитовидной железе и селезенке быка (Gorup — Besanez), в
некоторых патологических эксудатах (Heintz, Brieger), в моче кроликов, кормимых
морковью (Meissner и Jolly; ср. Salkowski) и людей, после спаржи (Hilger). Я.
кислота получена при окислении азотной кислотою: стеариновой кислоты (Bromeis),
японского (Sthamer) и пчелиного (Ronalds) воска,
спермацета (Radcliff); кислот: себациновой, азелаиновой (Аrрре), масляной
(Dessaignes; из последней она получена и при действии воды и брома (?) при 210°,
Friedel, Machuca); при плавлении с едкими щелочами: гуммиарабика, молочного
сахара, карминовой кислоты (Hlasiwetz, Grabowski); образование Я. кислоты
наблюдено: при спиртовом брожении глюкозы (Pasteur), при брожении (под влиянием
дрожжей) аспарагина (см.; Piria), яблочнокислого кальция (см. Яблочная кисл.,
Dessaignes, Liebig), виннокислого аммония (K öni g);
при действии Bacillus lactis aerogenes на яблочную кислоту (Emmerling); при
гниении мяса (Е. и H. Salkowski), печени (Ekunia), из фибрина под влиянием
стрептококков (Emmerling; ср. кроме того Fitz). Других синтетических реакций ее
образования можно и не перечислять, так как они все уже приведены выше при
перечислении реакций образования Я. кислот (Schmitt, Dessaignes, Kekul é,
Simpson, Wichelhaus, Bandrowski, Бишоф, Steiner, Walker и Brown). Для добывания
Я. кислоты прибегают или к перегонке янтаря (acidum succinicum officinale), или
же к брожению виннокислого аммония (K ö nig).
Я. кислота кристаллизуется в одноклиномерных призмах или пластинках; имеет
слабокислый, неприятный вкус; плавится при 185° (Давыдова); при 760 мм. давления
кипит, распадаясь на воду и ангидрид, при 235°; образования CO 2
при этом не наблюдено; распадение на СО 2
и пропионовую кислоту: HO 2C.C2H4.СО 2 Н
= СО 2 + СН 3.СH 2.СО 2 H,
идет, однако, при действии солнечного света на водный раствор Я. кисл. в
присутствии солей окиси урана (Seekamp); ср. Предельные органические кисл.,
реакцию May. Я. кисл. не изменяется под влиянием HNO 3,
СrО 3 или хлорной
воды; МnО 2 с Н 2 SО 4
дают уксусную кислоту; при
плавлении с КОН наблюдается щавелевая кисл. Пятихлористый фосфор последовательно
(Kauder) образует с Я. кисл.: ангидрид С 2H4.С 2 О 3
и хлористый сукцинил
(несимметричный, иначе двухлоробутиролактон —
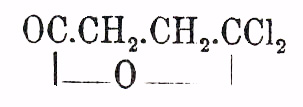
(Gerhardt, Chiozza; Mö ller,
Auger; cp,однако D. Vorl ä nder,
"Berl. Ber.", 30, 2268 примеч. [1897], о возможности для него симметричной
формулы, т. e.C lOC.CH2.CH2.COCl);
при одновременном действии пятихлористого фосфора и хлора образуются еще:
хлористый фумарил (и хлорангидрид малеиновой кислоты) и, в конце концов,
гексахлорэтан — Сl 3 С.ССl 3
(Kauder). О случаях
образования ангидрида Я. кисл. упомянуто выше; для добывания его удобно
недолговременное кипячение Я. кислоты с хлористым ацетилом (A ü schutz;
об изменении ангидрида при долговременном нагревании см. Volhard); это
кристаллическое вещество, плав. при 120°, кипящее с некоторым разложением
(выделение CO 2 и
образование дилактона ацетодиуксусной кисл. — СО(СН 2.СН 2.СО 2 Н) 2,
Volhard) при 261°; обладает особым слабым, действующим раздражающим образом на
слизистые оболочки носа, запахом; в отличие от кислоты легко растворим в
хлороформе; при лежании во влажном воздухе притягивает воду, превращаясь в
кислоту; легче идет реакция при кипячении с водой; со спиртами дает
соответственные сложные эфиры, с аммиаком и первичными жирными аминами —
соответственные аминокислоты, с анилином (толуидином и т. д.) — анилокислоту
(см. выше); анилокислоты легко кристаллизуются и служат для характеристики Я.
кислоты. При нагревании аминокислоты и анилокислоты теряют элементы воды,
превращаясь в имиды (замещенные имиды). Сукцинимид
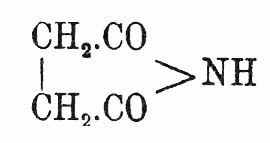
плавится при 126° и кипит при 288°; кристаллизуется с 1H 2 O
и является слабой кислотой, способной замещать имидный водород металлами.
Многочисленные галоидные производные Я. кисл. получены главным образом не из
самой Я. кислоты, а из яблочной и винной кислот замещением их спиртовых, водных
остатков галоидами, или же присоединением галоидоводородов, галоидов к
малеиновой и фумаровой кислотам; возможны и известны в многочисленных
видоизменениях, так как моногалоидоянтарная кислота НО 2 С.СНХ.СН 2 СО 2 Н
содержит один асимметричный углеродный атом, а в симметричнодвузамещенных
кислотах общей формулы НО 2 С.СНХ.СНХ.СО 2 Н
— их два. О продуктах взаимодействия Я. кисл. с альдегидами и кетонами см.
Параконовые кисл. Из гомологов Я. кисл. укажем на пировинную кис. НО 2 С.СH(СH 3).СН 2.СО 2 Н
и пимелинов. кис. НО 2 С.СН[СН(СН 3)2 ].СН 2.СО 2 Н
(см.). Первая, содержа один асимметричный атом С, известна в трех видоизменениях
(ср. выше); из них давно открыта рацемическая пировинная кисл. (пара-кислота,
см. Винная кислота), образующаяся при сухой перегонке винной кисл. (Fourcroy и
Vanquelin) или при действии на них концентрированного НСl при 180° (Genther,
Riemann); она же образуется из пировиноградной при нагревании ее до 170° или
действии НСl при 100° (B ö ttinger).
Реакция, по-видимому, идет таким обр., что из винной (виноградной кисл.) с
потерей элементов воды и СО 2
образуется оксиакриловая кисл.,
превращающаяся в момент образования в пировиноградную кисл.: НО 2 С.СH(OН).СН(ОН)CO 2 H
→ Н 2 O + СО 2
+ СН 2:С(ОН).СО 2 Н
(оксиакриловая кис.) → Н 2 О
+ CO 2 + CH3.CO.CO2 H
(пировиноградная кис.), а последняя конденсируется в кетовалерокарбоновую кисл.
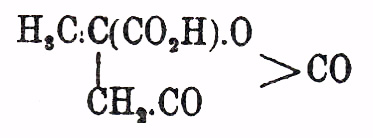
(L. A. 317), которая теряет СО 2,
и, присоединяя воду, образует, наконец, пировинную кисл: 2СН 3.СО.СО 2 Н-СО 2
= НО 2 С.СН(СН 3).СН 3.СО 2 Н.
О других возможных синтетических случаях образования пировинной кисл. см. выше.
Рацемическая пировинная кислота кристаллизуется в трехклиномерных призмах,
плавящихся при 112°. При нагревании легко дает ангидрид, плав. при 32° и кип.
при 247°. При кристаллизации кислой соли стрихнина удается разделить
рацемическую кислоту на правую и левую пировинные кислоты (Ladenburg).
Многочисленные галоидозамещенные производные пировинной кислоты получены
присоединением галоидоводородов (НСl, НВr) и галоидов к ита-, мезо-,
цитраконовым кислотам (см. Цитраконовая кислота). Симметричные двузамещенные Я.
кислоты образуются: 1) при гидрогенизации ангидридов двузамещенных малеиновых
кислот HJ, или амальгамой натрия (Otto и Beckurts, Bischoff и Voit); 2) из
моногалоидозамещенных одноосновных предельных кислот при действии серебра (H e ll
и Rothberg), или из тех же галоидозамещенных производных с помощью KCN и C nH2n+1 J
(см. выше; Н. Зелинский); 3) из соответственных производных ацетоуксусного эфира
(см. выше 9-ую общую реакцию образования Я. кислот), и 4) из соответственных
трикарбоновых (малонкарбоновых) кислот при нагревании с крепкой соляной кисл.
(Bischoff). Полученную смесь изомеров делят кристаллизацией из воды. Все эти
кислоты известны в двух видоизменениях: пара- и антикислотах, природа которых
еще не разъяснена. Симм. диметилянтарная кис. НО 2 С.СH(СН 3)СН(CН 3).СО 2 Н
— пара-, плав. при 192—194°; при долговременном нагревании распадается отчасти с
образованием смеси ангидридов пара- и антикислот; антикислота плав. при
120—123°; при нагревании с соляной кислотой при 190° превращается в паракислоту;
другие гомологи отличаются только темпер. плавления и растворимостью, но их
взаимные отношения те же. Неизвестно, имеются ли тут случаи монотропии или
энантиотропии (ср. Фосфор и Фумаровая кислота).
А. И. Горбов.
|