Щавелевая кислота
— этандикислота (Oxals ä ure,
acide oxalique), получена впервые в 1773 г. Совари из кисличной соли (кислая
щавелево-калиевая соль); Бергман получил ее окислением сахара азотной кислотой и
описал под именем сахарной кислоты; Шееле в 1776 г. установил идентичность обеих
кислот. IIриготовление Щ. кислоты из
сахара было первым случаем
получения органического соединения вне организма. В свободном состоянии Щ.
кислота вообще в природе встречается редко, до сих пор найдена только в грибе
Boletus sulfureus; в виде солей находится в растениях и продуктах животного
царства. В виде кислого
щавелекислого калия — в соке видов oxalis — кислиц. Чаще всего Щ. кислота
встречается в растениях в виде кристаллических отложений кальциевой соли внутри
клеток. Кальциевая соль Щ. кислоты составляет часть мочи и выделений некоторых
желез. Аммонийная соль Щ. кислоты, как продукт разложения мочевой кислоты,
находится в гуано. Щ. кислота, кроме того, образует некоторые минералы, как
вевеллит и тиршит (щавелекислая известь), которые найдены в виде накипи на
исландском шпате и мраморе, и гумбольдит (щавелекислая закись железа), найденный
в некоторых буроугольных месторождениях. Щ. кислота имеет состав, эмпирически
выражаемый C 2H2O4,
она дает два ряда солей, зефиров и проч., т. е. двуосновна, и заключает две
гидроксильных или карбоксильных группы. Строение ее может быть выражено
HOOC—COOH. Кристаллизуется с 2-мя частицами воды С 2 Н 2 О 4 ∙2Н 2 О,
что соответствует полному гидрату (OH) 3C—C(OH)3
(Штауб и Ватсон Смит). Строение ее подтверждается реакциями получения, из
которых теоретически интересны: 1) образование Щ. кислоты при действии CO 2
на расплавленный натр при 360° (Дрексель), при чем образуется натриевая соль Щ.
кислоты:
CO2—CO2 + 2Na = NaOOC—COONa.
2) Щ. кислота получается при нагревании до 400° муравьино-калиевой или
натриевой соли:
2HСО 2Na = 2H +
СО 2 NaСО 2Na.
3) Циан CNCN, как нитрил Щ. кислоты, при действии омыляющих веществ дает амид
Щ. кислоты (оксамид) NН 2COCONH2,
а последний легко — Щ. кислоту. 4) При осторожном окислении муравьиной кислоты
получается Щ. кислота. 5) Перхлорэтан C 2Cl6
при продолжительном нагревании с едким кали переходит в Щ. кислоту. 6)
Окислением сложных органических соединений, для каковой цели употребляют или
обработку азотной кислотой или сплавление с едкими щелочами. Последние 2 метода
служат для фабричного производства Щ. кислоты. Щ. кислота кристаллизуется из
воды в бесцветных одноклиномерных, сильно двупреломляющих призмах, с двумя
молекулами воды (С 2 Н 2 О 4 ∙2Н 2 О),
которые теряет при 100° или при стоянии над серной кислотой. Плавится при
101,5°. Безводная кислота при 100° возгоняется, выше 150° С разлагается на воду,
углекислоту, окись углерода и муравьиную кислоту, при быстром и сильном
нагревании — на воду, окись углерода и углекислоту. Безводная кислота плавится в
капиллярных трубках при 189°. Щ. кислота растворима в воде, спирте и эфире. 100
частей воды растворяют при 20° 8,8 частей безводной кислоты, 100 частей
безводного спирта при 15° — 23,73 частей, 100 частей эфира — 1,27 частей. При
нагревании с крепкой серной кислотой Щ. кислота распадается на воду, углекислоту
и окись углерода. Легко отдающими свой кислород окислителями Щ. кислота
окисляется нацело, до СО 2:
С 2 Н 2 О 4
+ О = 2СО 2
+ Н 2 О;
так действует нагревание с азотной кислотой, хлорноватистой, йодной,
хромовой, хлорными соединениями золота и платины (выделяются металлы); на
холоде, легко — марганцевой кислотой в кислом растворе (реакция применяется в
объемном анализе). Щ. кислота, как двухосновная, дает с одноатомными металлами
два ряда солей, 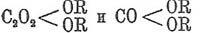 ,
в зависимости от того, сколько атомов водорода замещаются металлом. Кроме этих
двух рядов нормальных солей, она дает легко малопрочные надкислые соли —
соединение кислой соли Щ. кислоты с частицей кислоты, напр. C 2 О 4HNaC2 О 4 Н 2.
Двухатомные металлы дают средние соли, кислые соли их малопостоянны и легко
распадаются с выделением Щ. кислоты. Составь тех и других выражается: ,
в зависимости от того, сколько атомов водорода замещаются металлом. Кроме этих
двух рядов нормальных солей, она дает легко малопрочные надкислые соли —
соединение кислой соли Щ. кислоты с частицей кислоты, напр. C 2 О 4HNaC2 О 4 Н 2.
Двухатомные металлы дают средние соли, кислые соли их малопостоянны и легко
распадаются с выделением Щ. кислоты. Составь тех и других выражается:
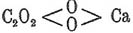
средняя кальциевая соль
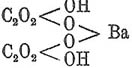
кислая бариевая соль
Гораздо постояннее кислых солей легко образующиеся двойные соли с
одноатомными металлами, напр.
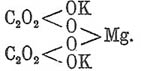
С окислами М 2 О 3
Щ. кислота образует ряд двойных солей K 6Fe2 (С 2 О 4)6∙6H2 О,
K 6Cr2 (С 2 О 4)6∙6H2 О,
K 2Cr2 (С 2 О 4)4∙10H2 О
и т. д. Они представляют соли соответствующих комплексных кислот. Большинство
солей Щ. кислоты кристаллизуется с водой, которая более или менее легко
выделяется. В воде легко растворимы только соли щелочных металлов, большинство
солей совсем нерастворимо, в спирте растворима только литиевая соль. При
нагревании соли Щ. кислоты разлагаются или на углекислую соль и окись углерода,
или на окись металла, углекислоту и окись углерода, или на металл и углекислоту
в зависимости от постоянства углекислых солей металлов при условиях реакции
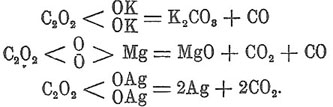
Техническое значение из солей имеют: кислая щавелевокислая соль калия с
примесью надкислой соли, употребляющаяся для удаления чернильных и ржавчинных
пятен; действие основано на образовании двойной растворимой соли окиси железа и
калия; K 2 Fe(С 2 О 4)2∙H2 О
— двойная соль калия и закиси железа употребляется в фотографии как проявитель,
приготовляется смешением растворов железного купороса и средней
щавелево-калиевой соли; двойные соли сурьмы калия и натрия употребляются как
протравы в красильном деле. Самая характерная соль Щ. кислоты есть кальциевая —
С 2 О 4 Са,
нерастворимая в воде и уксусной кислоте, но растворимая в соляной и азотной; в
виде этой соли определяются при анализе кальций и Щ. кислота. Щ. кислота дает
многочисленные производные. Ангидрид Щ. кислоты неизвестен. Хлорангидрид
СlСОСОСl обыкновенным путем, т. е. действием пятихлористого фосфора
на кислоту, не получается, Щ.
кислота дает при этом воду, углекислоту, окись углерода и хлорокись фосфора.
Хлорангидрид получается действием пятихлористого фосфора на средний эфир
этилового спирта. Щ. кислота, как двухосновная, дает два ряда сложных эфиров со
спиртами, из эфиров имеют значение диметилщавелевый СН 3 ОСОСООСН 3,
кристаллический, с точкой плавления +54, употребляется для очистки метилового
спирта. Соответствующий эфир этилового спирта представляет жидкость. Нитрил Щ.
кислоты есть циан CNCN (см. это соединение). Амидов два — оба известны.
Оксамид NH 2COCONH2
получается при омылении циана и
отщеплением воды от аммиачной соли Щ. кислоты при нагревании, в виде белого, в
воде, спирте и эфире трудно растворимого порошка. Оксаминовая кислота NH 2COCOOH
при нагревании кислой щавелево-аммиачной соли растворима в спирте и эфире
(подробнее см. Оксамид, Оксаминовая кислота). Имид Щ. кислоты СО—
NH—СО, оксальимид, получается нагреванием оксаминовой кислоты с пятихлористым
фосфором или с хлорокисью фосфора, представляет кристаллически хорошо
образованные блестящие призмы, трудно растворимые в холодной воде, с нейтральной
реакцией, легко растворим в слабом аммиаке, при кипячении с водой дает оксамид и
Щ. кислоту, с крепким раствором аммиака дает оксамид.
Заводское производство Щ. кислоты основано на окислении различных
органических веществ и отбросов азотной кислотой или едкими щелочами. При
фабрикации посредством азотной кислоты исходным материалом служат дешевые сорта
сахара: глюкоза, полученная из крахмала, или отбросы с сахарных заводов;
последние выгоднее употреблять, так как стоимость равного количества сахара в
отбросах сахарного производства будет меньше, чем того же количества глюкозы,
особенно если употреблять патоку с песочных заводов, которая, кроме того,
заключает большое количество калийных солей, вполне утилизируемых при обработке.
Ход работы следующий: в глиняных или деревянных, выложенных свинцом сосудах,
помещенных в большую водяную баню из кирпича или камня на цементе, с паровым
нагревателем, обрабатывают патоку азотной кислотой уд. в. от 1,2 до 1,27 при
нагревании до 50° С. На 125 частей продажной патоки или на 100 частей сахара
берут 443 части азотной кислоты. При надлежащей температуре и крепости кислоты
реакция идет спокойно, с выделением окиси азота, которая по трубам проводится в
серные камеры, если есть они на заводе, или, смешиваясь на пути с воздухом и
паром, в различного устройства конденсационные приборы. Прибавление небольших
количеств серной кислоты к азотной способствует реакции. По окончании выделения
газов жидкость спускается в кристаллизационные ящики. Выкристаллизовавшаяся
кислота промывается холодной водой, сушится и поступает в продажу. 100 частей
сахара дают около 115 ч. кристаллической кислоты. Этот способ, несмотря на всю
его простоту и легкость
ведения самого процесса, редко применяется, так как очень дорог вследствие
употребления окислителем дорогой азотной кислоты, переходящей при реакции в
низшие окислы азота, регенерация которых очень затруднительна и дорога; самой
лучшей утилизацией
выделяющихся окислов являлось бы применение их для камерного процесса, но этому
сильно мешает, во-первых, неравномерность выделения газов, обильное в начале
реакции и незначительное в конце ее, что для камерного процесса вредно,
во-вторых, сравнительно небольшая трата окислов азота при современном камерном
процессе благодаря их постоянному улавливанию в башнях. Сплавлением с едкими
щелочами получение Щ. кислоты хотя и более трудно, но зато значительно дешевле,
так как исходным материалом служат
отбросы, почти не имеющие цены,
главным образом опилки, а едкие щелочи нацело регенерируются, конечно, кроме
неизбежных при всяком производстве потерь. Прежде чем перейти к описанию
заводского процесса в том виде, как он ведется на фабриках, необходимо подробнее
рассмотреть действие едкого калия и натрия на растительную клетчатку различного
происхождения и при разных условиях. Образование Щ. кислоты при сплавлении
органических веществ со щелочами было замечено в 1829 г. Гей-Люссаком,
технически способ впервые был разработан Поссоцом (Possoz), и он же ввел его в
заводскую практику. Поссоц при своих опытах заметил: 1) что едкие кали и натр
относятся неодинаково к реакции, именно, что при сплавлении с едким натром
получается гораздо меньше кислоты, чем если сплавлять с едким кали, причем в
первом случае окисление органических соединений идет до СО 2.
2) Что смесь обеих щелочей в известной пропорции оказывает наиболее
благоприятное влияние на ход реакции с образованием наибольшего количества Щ.
кислоты. Так, если обозначить через 100 количество Щ. кислоты, образующейся при
действии чистого едкого кали на крахмал, то при различных отношениях между
основаниями получим:
| NaHO+ KHO |
получается С 2 Н 2 О 4 |
| — + 100 |
100 |
| 25 + 75 |
110 |
| 33 + 67 |
112,5 |
| 50 + 50 |
100 |
| 67 + 33 |
90 |
| 75 + 25 |
80 |
| 100 + — |
незначительное
количество |
3) Поссоц заметил, что органические вещества растительного происхождения дают
большие выходы Щ. кислоты, чем животного. Последующими опытами Торна было
установлено: наиболее благоприятная температура реакции 240° С, соотношение
между количеством опилок и едкими щелочами, именно 1:2, состав едкой щелочи
(40КНО + 60NaHO); кроме того, выяснено, что прибавка к плавящейся массе
окислителей, вроде перекиси марганца, улучшает выходы Щ. кислоты, что древесные
опилки как лиственных, так и хвойных пород дают почти одинаковые количества Щ.
кислоты, хотя лиственные вообще большие, и что процесс следует вести, по
возможности распределяя массу, назначенную для обработки, тонким слоем, чтобы
усилить окисление и предохранить самонагревание массы, последствием чего
является значительное ухудшение выходов Щ. кислоты, как ясно видно из следующей
таблицы:
|
КНО |
NaHO |
при работе |
|
в толст. слое |
в тонком |
| 20 |
80 |
30,04 |
74,76 |
| 30 |
70 |
38,89 |
76,77 |
| 40 |
60 |
43,70 |
80,57 |
| 60 |
40 |
42,64 |
80,08 |
| 80 |
20 |
61,32 |
81.24 |
| 100 |
— |
65,51 |
81,23 |
Основываясь на опытах Поссоца и Торна в настоящее время готовят Щ. кислоту
следующим образом: обливают воздушно-сухие опилки кипящим едким щелоком уд. веса
1,3 до 1,4, употребляя на 1 часть опилок 2 части щелочей (40KHO + 60NaHO),
нагревают смесь в железных, плоских, около 2 м диаметром чашах при постоянном
механическом помешивании до 240° C, наблюдая, чтобы толщина слоя не превосходила
1,5—2 стм. По мере нагревания сначала испаряется вода, масса становится
темно-бурой, появляется своеобразный запах, при 180° окраска массы начинает
переходить в желтовато-зеленый цвет, и опилки мало-помалу теряют свою древесную
структуру, которая к концу реакции совсем исчезает. Горячий сплав выщелачивают
кипящей водой, концентрируют полученный раствор до 38° В., охлаждают, при чем
кристаллизуется почти вся Щ. кислота в виде щавелево-натриевой соли; кристаллы
отделяют центрифугой от маточного рассола, который содержит в себе мало Щ.
кислоты, углекислые, едкие щелочи и органические вещества. Кристаллы
щавелево-натриевой соли перерабатываются на Щ. кислоту, а из маточных солей
регенерируются заключающиеся в них щелочи, для чего щелочи переводят
прибавлением извести — в едкие; полученный раствор, содержащий гуминовые
вещества, упаривается досуха, и сухой остаток обжигается при доступе воздуха,
при чем получаются углекислые кали и натр, которые идут снова в дело для
приготовления едких щелочей. Кристаллы щавелево-натриевой соли растворяются в
горячей воде, к раствору при постоянном помешивании и подогревании прибавляют
известкового молока до полного осаждения Щ. кислоты. Полученный при этой
операции едкий натр идет снова в работу, а щавелево-известковая соль
подвергается дальнейшей обработке. Для выделения Щ. кислоты щавелево-известковую
соль при слабом нагревании паром обрабатывают при постоянном помешивании слабой
серной кислотой 15—20° В. (1 ч. соли, 2 ч. Н 2SO4
при 66° C), при чем выделяется гипс, а Щ. кислота остается в растворе. Осадок
гипса отделяют на центрифуге или, еще лучше, на фильтр-прессе и промывают.
Раствор содержит, кроме Щ. кислоты, серную кислоту и гипс, для выделения
которого раствор осторожно паром концентрируют до 15° В. летом, до 10° В. —
зимой и охлаждают, гипс после 3-4-часового стояния выкристаллизовывается. Слитый
с кристаллов гипса раствор упаривают до 30° В. и кристаллизуют из него Щ.
кислоту. Кристаллы Щ. кислоты для очищения подвергаются повторной
кристаллизации; маточный рассол, содержащий Н 2SO4,
употребляется снова при обработке щавелево-кальциевой соли. Полученная после
перекристаллизации Щ. кислота для техники достаточно чиста и содержит около
процента серной кислоты и солей калия и натрия. Интересное видоизменение этого
распространенного способа патентовано Капитеном и Гертлингом, именно смесь из
20-ти частей опилок, 1,5 частей тяжелых углеводородов (машинного или
вазелинового масла) с 40 частями едкого натра в растворе уд. веса 1,35 В. плавят
при 200° С., причем реакция идет спокойно, с выделением воды и углеводородов; по
прекращении выделения последних масса принимает желтый цвет и оказывается
содержащей от 42—43 % Щ. кислоты, или, другими словами, из 100 ч. древесной
массы получается до 143 ч. Щ. кислоты. При этом способе почти не образуется
гуминовых веществ, и осаждающаяся при дальнейшей работе щавелево-известковая
соль выпадает совсем белой. Кроме того, Щ. кислоту, по Ниттлю (Nittl), добывают
нагреванием с едким натром отбросных щелоков при сульфитном процессе добычи
клетчатки. По Лившицу и Берштейну, получающиеся при обработке дерева на
целлюлозу смесью серной и азотной
кислот (32 % Н 2SO4,
18—20 % NНО 3 и 50
% H 2 O) отбросные
кислоты заключают много Щ. кислоты, которую можно нацело получить
кристаллизацией, причем из 100 ч. дерева получают от 38—40 % целлюлозы и около
30 % Щ. кислоты. Щ. кислота в технике имеет довольно значительное применение:
она употребляется при крашении бумажных, шерстяных и шелковых тканей как
протрава; при приготовлении чернил (для растворения берлинской лазури),
розоловой и муравьиной кислот, декстрина, при белении и очищении стеарина.
Н. Тутурин.
|