Пиразины
Вернее, пирадиазины, иногда также называются пиазинами — могут
быть рассматриваемы как ароматические углеводороды, в которых две группы СН
бензольного кольца, находящиеся в пара-положении, замещены двумя атомами азота,
следовательно, конституционная формула простейшего из них будет
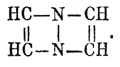 . По своему
химическому характеру П. являются весьма слабыми двухатомными основаниями, соли
которых легко разлагаются содой и имеют нейтральную реакцию. Характерны для П.
их двойные соли с HgCl 2, AuCl3,
которые приближают их к пиридинам (см.) и к истинным аммиачным основаниям. При
восстановлении натрием в спиртовом растворе П. присоединяют 3Н 2
и переходят в пиперазины. Простейшие П. образуются: 1) конденсацией
амидокетонов или амидоальдегидов с выделением 2 частиц воды и одновременным
окислением образующегося первоначально продукта конденсации при помощи сулемы
HgCl 2; вместо
амидокетонов можно брать изонитрозокетоны, их восстановить и, не изолируя
продукта восстановления, прямо перегонять полученный раствор с сулемой: . По своему
химическому характеру П. являются весьма слабыми двухатомными основаниями, соли
которых легко разлагаются содой и имеют нейтральную реакцию. Характерны для П.
их двойные соли с HgCl 2, AuCl3,
которые приближают их к пиридинам (см.) и к истинным аммиачным основаниям. При
восстановлении натрием в спиртовом растворе П. присоединяют 3Н 2
и переходят в пиперазины. Простейшие П. образуются: 1) конденсацией
амидокетонов или амидоальдегидов с выделением 2 частиц воды и одновременным
окислением образующегося первоначально продукта конденсации при помощи сулемы
HgCl 2; вместо
амидокетонов можно брать изонитрозокетоны, их восстановить и, не изолируя
продукта восстановления, прямо перегонять полученный раствор с сулемой:
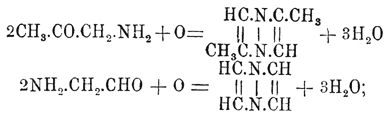
образующиеся соединения по исходным материалам называют также алдинами и
кетинами; 2) конденсацией в присутствии аммиака и последующим окислением α-хлор-
или бромкетосоединений; очевидно, что этот синтез основан на промежуточном
образовании амидокетонов:
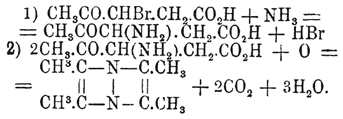
Дифенилпиразины получаются из производных дифенилдигидропиразинов.
Представителями простейших П. могут служить П. C4H4N2,
твердое кристаллическое вещество, пахнущее гелиотропом, летучее при обыкн.
темп., плавящееся при 55° и кипящее при 115°, αγ -диметилпиразин,
или кетин С 4 Н 2 (СН 2)N2,
масло, кипящее при 153°, и αγ -дифенилпиразин,
плавящийся при 196° и не перегоняющийся без разложения. При окислении
марганцово-калиевой солью гомологов П. с жирными боковыми цепями получаются
пиразинкарбоновые кислоты, характерные тем, что они при простом нагревании
выделяют углекислоту и переходят в П. Раньше было указано, что при
восстановлении в щелочном растворе П. переходят в гексагидропиразины, или
пиперазины. Но теоретически допустимы и промежуточные стадии гидрогенизации; они
в действительности и получены, хотя и не прямым путем. Теоретически возможны три
вида дигидропиразинов:
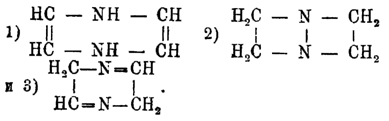
Первые получаются конденсацией 2 частиц замещенных α-амидокетонов или 2 част.
α-бромкетонов с 2 част. первичных аминов или анилинов; очевидно, что второй
способ является только видоизменением первого:
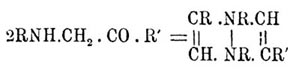
Из этого класса соединений интересны только фенильные производные, напр.,
п-дибензил-α, γ - дифенилдигидропиразин,
в котором R = С 6H4 —СН 3
и R' = C 6 H5. Эти
соединения легко отщепляют группы R и переходят в дифенилпиразины.
Соединения, принадлежащие ко второму типу дигидропиразинов, получаются из
этилендиамина и 1,2-дикетонов:
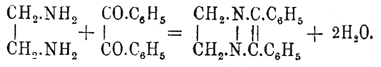
α, γ-Дигидропиразины до
сих пор еще не получены. Из возможных двух типов тетрагидропиразинов
известен только один в виде своего производного п-дифенилтетрагидрофенилпиразина
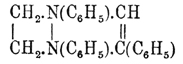 , который
получается конденсацией этилендифенилдиамина с бромацетофеноном. CH 2Br.CO.C6H5.
Гексагидропиразины, или
пиперазины, представляют уже вполне насыщенные соединения и потому по своему
химическому характеру отвечают соответствующим жирным соединениям, т. е. они
являются уже типическими жирными дииминами, или вторичными диаминами (см.), и
настолько же далеко отстоят от П., насколько гексагидроароматические соединения
от ароматических. Пиперазины получаются или восстановлением П. натрием в
спиртовом растворе, или конденсацией хлористоводородных солей алкилендиаминов,
или же, наконец, конденсацией первичных аминов и алкилендиаминов с
дибромэтиленом: , который
получается конденсацией этилендифенилдиамина с бромацетофеноном. CH 2Br.CO.C6H5.
Гексагидропиразины, или
пиперазины, представляют уже вполне насыщенные соединения и потому по своему
химическому характеру отвечают соответствующим жирным соединениям, т. е. они
являются уже типическими жирными дииминами, или вторичными диаминами (см.), и
настолько же далеко отстоят от П., насколько гексагидроароматические соединения
от ароматических. Пиперазины получаются или восстановлением П. натрием в
спиртовом растворе, или конденсацией хлористоводородных солей алкилендиаминов,
или же, наконец, конденсацией первичных аминов и алкилендиаминов с
дибромэтиленом:
1) C4H4N2
+ 3Н 2 = C4H10N2;
2) 2HClNH2—CH2CH2NH2—HCl =
HCl—NH=(CH2—CH2)2=NH—HCl + 2NH4Cl;
3a) 2ВrСН 2 СН 2Br
+ 2C6H5NH2 = C6H5N=(CH2CH2)=NC6H5
+ 4HBr
3b) NH2CH2CH2NH2 + BrCH2CH2Br
= HBrNH=(CH2CH2)2=NH—HBr.
Простейший член этого ряда соединений, пиперазин, или
диэтилендиамин, NH=(CH2—CH2)NH,
был впервые получен в 1856 г. Натансоном из хлористого этилена и аммиака.
Пиперазин кристаллизуется из спирта в ромбич. листочках, плав. при 104° и
перегоняется при 145—146° без разложения. Получать его можно всеми
вышеуказанными для пиперазина реакциями, но легче всего, по-видимому,
разложением щелочами динитрозо-п-дифенилпиперазина, который при этом
распадается на 2 мол. нитрозофенола и пиперазин. Действуя монохлороуксусной или
щавелевой кислотами на замещенные этилендиамины или конденсируя замещенные
глицины, можно получить кето- и дикетопиперазины, весьма тщательно исследованные
Бишоффом. Бензо-П. — см. Хиноксалины.
Д. А. Хардин. Δ .
|