Парафины
(хим.) — предельные (см. Замещение, Предельные соединения) углеводороды ряда
C nH2n+2.
П. встречаются в значительном количестве в природе; низшие члены ряда выделяются
во многих местностях из почвы (напр. в Америке — в Пенсильвании, у нас на
Кавказе, близ Баку, в Крыму близ Бунганака и т. д.); следующие члены составляют
главную массу амер. нефти (см. соотв. ст.) и встречаются в значительном
количестве в нефти челекенской и закаспийской (Уоррен, Пелуз, Кагур, Шорлеммер,
Харичков) и, наконец, высшие входят в состав канадской нефти (Болей) и различных
минералов каменноугольной системы, залежей бурых углей и битуминозных сланцев и
известны под названием озокерита
(см.), горного воска и т. д. (см. о
лекене); особняком стоит нахождение одного из П.(нормального гептана) в
калифорнийской сосне — Pinus sabiniana (Торпе, Шорлеммер [Существуют указания на
присутствие П. в розовом масле (?) и в цветах Crysantbemum cinerar i nefolium
(? Цукко).]). Образуются П. при сухой перегонке дерева, торфа, бурых и каменных
углей, битуминозных сланцев (Гревиль Вильямс, Шорлеммер), смол (Ренар), животных
остатков, жирных масел, кальциевого мыла из жира рыбы Alosa Menhaden, П.
собственно (Торпе и Юнг), многих других органических веществ (см. ниже) и при
растворении в кислотах чугуна (Клоэз, наряду с нафтенами?). Реакциями получения
П являются: 1) замещение в предельных галоидангидридах спиртов С nH2n+1 X
(Х = Сl, Вr, J) галоида водородом и восстановление жирных предельных кислот С nH2n О 2
и кетонов С n-1 Н 2n СО;
2) действие воды (кислот) на предельные металлоорганические соединения; 3)
присоединение водорода к олефинам (см.): C nH2n + H2
= CnH2n+2; 4)
отнятие элементов углекислоты от предельных жирных кислот: (С nH2n+1)СО 2H
— CO2 и C nH2n (СО 2H)2
— 2CO2 = CnH2n+2;
5) действие натрия (или цинка) на предельные галоидангидриды спиртов
(преимущественно йодюры): С nH2n+1 J
+ С mH2m+1 J
+ 2Na = (С nH2n+1)С mH2m+1
+ 2NaJ и 6) электролиз жирных кислот (их солей):
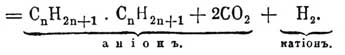
При первой реакции действуют на С n Н 2n+1 X
водородом в момент выделения, для чего употребляют или амальгаму натрия (также
цинк с соляной кисл., цинк с водой при 150° — 160°; Франкланд), напр.: С 2H5J
+ H2 = C2H6
+ HJ, или цинкмедную пару (в присутствии спирта или воды — Гладстон и Трайб),
или же нагревают йодангидрид [В этом случае С nH2n+1 J
можно заменить спиртом СH 2n+1 (OH).]
с йодистым водородом (Бертело): C 2H5J + HJ = C2H6
+ J2 [Реакция,
по-видимому, ведет иногда к продуктам, изомерным с теми, которые должны бы
были образоваться (ср.
Полиметиленовые углеводороды); так
из
маннита (см.) при восстановлении
его йодистым водородом получается симметричный диметилбутан —
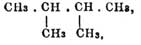 , который
образуется и из диаллила(см., Бертело).] или с хлористым алюминием (Кёнлейн).
Последний способ ведет к различным продуктам, смотря по темп., при которой
происходит взаимодействие С nH2n+1 J
с AlCl 3
[Нагревание производят в запаянных трубках, как при восстановлении С nH2n+1 J
йодистым водородом . ];
всегда образуются при этом П., и первоначально П., отвечающий взятому
йодангидриду, т. е. из йодистого бутила — бутан, из йодистого гексила — гексан и
т. д., но высшие члены ряда (до пентана) под влиянием АlСl 3
и образующегося HJ претерпевают, около 125° — 140°, распадение, ведущее к
образованию бутана, а этот последний в свою очередь, при температурах 160° —
225°, распадается, превращаясь в пропан; С 3 Н 8
в указанных условиях не изменяется (Лотар, Мейер и Клуге). Что касается
восстановления йодистым водородом предельных кислот, то эта реакция применима
только к получению высших П., начиная с нормального нонана С 9 Н 20,
т. е. с пеларгоновой кисл. (см.; Крафт): C nH2nO2
+ 6HJ = CnH2n+2 + 2H2O = 3J2.
Нагревают для этого в запаянных трубках 2—4 гр. кислоты с 3—4 ч.
йодистоводородной кислоты (уд. в. 1,7) и 1/3 ч. фосфора [Прибавление фосфора
облегчает ход реакции, так как в присутствии воды он превращает выделяющийся йод
в йодистый водород 2P + 3J 2 + 6H2O = 2P(OH)3
+ 6HJ. Фосфористая кислота претерпевает при этом отчасти дальнейшее изменение.]
3—5 часов при 210° — 249°; затем трубки вскрывают, прибавляют в них немного
фосфора и снова греют при той же температуре; операцию повторяют раза 2—3;
образованный П. перегоняют с водяными парами и нагревают с концентрированным
едким кали (Крафт). Выход не
особенно хороший и в этом отношении гораздо выгоднее восстановление йодистым
водородом в тех же условиях кетонов, которые должны быть, однако, предварительно
превращены — действием пятихлористого фосфора — в тела общей формулы С n Н 2nCl2
(см. Кетоны). К реакции образования П. из йодюров, при нагревании с водой и
цинком (см. выше): 2С n Н 2n+1J
+ 2Zn + 2H2O = 2CnH2n+2 + ZnJ + Zn(OH)2,
тесно примыкает реакция разложения цинкоорганических соединений водой; идет она
очень энергично и дает чистые продукты: Zn(C 2H5)2
+ 2H2O = 2C2H6 + Zn(OH)2
(Франкланд); меркурорганические
соединения дают П. только при действии кислот: Hg(C 2H5)
+ HCl = C2H6 + Hg(C2H5)Cl. , который
образуется и из диаллила(см., Бертело).] или с хлористым алюминием (Кёнлейн).
Последний способ ведет к различным продуктам, смотря по темп., при которой
происходит взаимодействие С nH2n+1 J
с AlCl 3
[Нагревание производят в запаянных трубках, как при восстановлении С nH2n+1 J
йодистым водородом . ];
всегда образуются при этом П., и первоначально П., отвечающий взятому
йодангидриду, т. е. из йодистого бутила — бутан, из йодистого гексила — гексан и
т. д., но высшие члены ряда (до пентана) под влиянием АlСl 3
и образующегося HJ претерпевают, около 125° — 140°, распадение, ведущее к
образованию бутана, а этот последний в свою очередь, при температурах 160° —
225°, распадается, превращаясь в пропан; С 3 Н 8
в указанных условиях не изменяется (Лотар, Мейер и Клуге). Что касается
восстановления йодистым водородом предельных кислот, то эта реакция применима
только к получению высших П., начиная с нормального нонана С 9 Н 20,
т. е. с пеларгоновой кисл. (см.; Крафт): C nH2nO2
+ 6HJ = CnH2n+2 + 2H2O = 3J2.
Нагревают для этого в запаянных трубках 2—4 гр. кислоты с 3—4 ч.
йодистоводородной кислоты (уд. в. 1,7) и 1/3 ч. фосфора [Прибавление фосфора
облегчает ход реакции, так как в присутствии воды он превращает выделяющийся йод
в йодистый водород 2P + 3J 2 + 6H2O = 2P(OH)3
+ 6HJ. Фосфористая кислота претерпевает при этом отчасти дальнейшее изменение.]
3—5 часов при 210° — 249°; затем трубки вскрывают, прибавляют в них немного
фосфора и снова греют при той же температуре; операцию повторяют раза 2—3;
образованный П. перегоняют с водяными парами и нагревают с концентрированным
едким кали (Крафт). Выход не
особенно хороший и в этом отношении гораздо выгоднее восстановление йодистым
водородом в тех же условиях кетонов, которые должны быть, однако, предварительно
превращены — действием пятихлористого фосфора — в тела общей формулы С n Н 2nCl2
(см. Кетоны). К реакции образования П. из йодюров, при нагревании с водой и
цинком (см. выше): 2С n Н 2n+1J
+ 2Zn + 2H2O = 2CnH2n+2 + ZnJ + Zn(OH)2,
тесно примыкает реакция разложения цинкоорганических соединений водой; идет она
очень энергично и дает чистые продукты: Zn(C 2H5)2
+ 2H2O = 2C2H6 + Zn(OH)2
(Франкланд); меркурорганические
соединения дают П. только при действии кислот: Hg(C 2H5)
+ HCl = C2H6 + Hg(C2H5)Cl.
Прямое соединение олефинов с водородом идет трудно (по Бертело около 500°) и
не ведет потому к образованию чистых продуктов; для газообразных олефинов в
присутствии платиновой черни оно возможно, впрочем, при обыкновенной температуре
(ф. Вильде); жидкие и твердые олефины могут быть превращены в П. (?) нагреванием
с йодистым водородом (Крафт). К числу нечистых реакций должна быть причислена и
реакция образования П. при нагревании со щелочами (натристой известью, баритом)
натриевых солей жирных кислот:
CH3—CO(ONa) + HONa = CH4 + CO(ONa)2, C6H12(CO2H)2
+ 2Ba(OH)2 = C6H14 + 2BaCO3 + 2H2 O,
так как одновременно с П. образуются кетоны (альдегиды?) и нек. другие продукты
сухой перегонки [Кроме того, получаются иногда изомерные углеводороды; так, при
перегонке энантовобариевой соли (см. Энантовая кислота) образуется не нормальный
гексан, а симметричный
диметилбутан (Риш).]; высшие жирные кислоты (их соли) даже совсем не образуют П.
при перегонке с натристой известью; в этом случае (напр. для кислот
миристиновой, пальмитиновой, стеариновой) могут быть, однако, получены хорошиe
выходы П., если натриевые соли этих кислот подвергнуть перегонке в пустоте с
метилатом натрия CH 3 (ONa)
(Май). При двухосновных кислотах реакция идет в две фазы, так как из себациновой
кислоты можно получить нониловую, а из янтарной — пропионовую кислоты (Май).
Отнятие галоида от двух молекул предельного йодюра и соединение остатков с
образованием П. было одной из первых синтетических реакций для них. Франкланд
(1848) нагревал для этого йодюр в запаянной трубке с цинком: 2C 2H5J
+ Zn = ZnJ2 + C4H10;
удобнее идет реакция, если действовать натрием на йодюр (Вюрц), разбавленный в
случае надобности безводным эфиром (или бензолом): 2C 2H5J
+ 2Na = 2NaJ + C4H10.
Если взята смесь двух йодюров, напр. йодистого этила и йодистого амила, то
имеет место и такая реакция: C 2H5J + C5H11J
+ 2Na = C7H16
+ 2NaJ; кроме того, понятно, образуются бутан C 4H10
и декан С 10 Н 22.
Это, впрочем, не единственные продукты реакции; побочно, как и при способе
Франкланда, образуются в небольшом количестве П. с меньшей частицей и олефины;
так, при нагревании цинка с йодистым этилом наблюдаются, кроме бутана, этан и
этилен: 2C 2H5J + Zn = ZnJ2 + C2H6
+ C2H4.
Реакция Франкланда несомненно протекает в несколько фаз: C 2H5J
+ Zn = C2H5—ZnJ, 2C2H5—ZnJ = (C2H5)2Zn
+ ZnJ2, (ср.
Металлоорганические соединения) и (C 2H5)2Zn
+ 2C2H5J = ZnJ2 + 2C4H10;
очень вероятно, что и при действии натрия на йодюры образуются промежуточные
металлоорганические соединения: C 10H21J + 2Na = C10H21—Na2J,
nC10H21—Na2J = (C10H21Na)n
+ nNaJ и, наконец, (C 10H21Na)n = (n/2)C20H42
+ nNa; в пользу такого представления говорит (по мнению Крафта и Гёттига)
покрытие натрия в начале реакции каким-то темно-синим кристаллическим веществом
(по Бертело — соединение калия с нафталином, а по Абельянцу — соединение калия с
бензолом представляют темно-синие, кристаллические вещества) и способность даже
сравнительно стойких металлоорганических соединений, как напр. меркуралкилов,
распадаться при нагревании (до 200°) на ртуть и П.: Hg(C 2H5)2
= Hg + C4H10
и Hg(C 8H17)2 = Hg + C16H34
(Эйхлер); нестойкость же натрорганических соединений явствует из невозможности
получения их в чистом виде (без примеси цинкорганических соединений). Как на
видоизменение только что описанного метода надо смотреть на реакцию
галоидангидридов спиртов с готовыми цинкорганическими соедин., как напр.: (CH 3)2Zn
+ 2CH3J = ZnJ2 + 2C2H6
(Франкланд), CH 3—CCl2—CH3
+ Zn(CH3)2 = ZnCl2 + C(CH3)4
(Львов), (CH 3)2CCl2 + Zn(C2H5)2
= ZnCl2 + (CH3)2—C—(C2H5)2
(Фридел и Ладенбург). Образование П. при электролизе солей жирных кислот
открыто (Кольбе) почти одновременно с реакцией Франкланда; первым полученным
таким образом П. был один из октанов: 2C 4H9—CO(OH)
= C8H18 + 2CO2 + H2.
Реакция имеет в настоящее время больше исторический интерес, так как получение
при посредстве ее углеводородов затруднительно; Крум-Броуну и Уокеру удалось
перенести ее на кислые эфиры двуосновных кислот и выработать элегантный,
синтетический метод образования двуосновных же кислот с большей величиной
частицы: 2C 2H5O—OC—CnH2n—CO(ONa)
= C2H5O—OC—C2H2n—CnH2n—CO—OC2H5
+ 2CO2 + 2Na. До
известной степени реакцию Кольбе напоминает случай образования этана при
нагревании перекиси ацетила с перекисью бария: CH 3—CO(O2)CO—CH3
= C2H6 + 2CO2
(Шютценбергер); образующийся здесь C 2H6
очень нечист (Дарлинг).
П., содержащие от 1 до 4 атомов углерода, газообразны при обыкн. темп., затем
до С 15 следуют
жидкости, за которыми являются твердые тела с постепенно возрастающей точкой
плавления. Судя по свойствам диметилпропана (см. ниже), должно думать, что и до
С 15 некоторые
углеводороды будут твердыми; так, по Львову и Храповицкому тетраметилбутан
(гексаметилэтан)
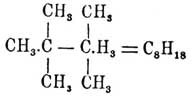
кристалличен, плавится при 96° — 97° и кип. при 105° — 106°. Точка кипения П.
одного строения быстро растет с увеличением частицы, так что высшие члены ряда
способны перегоняться без разложения только под уменьшенным давлением; как
всегда, частицы с нормальным строением (т. е. содержащие только два СН 3)
обладают высшей точкой кипения и, по мере нарастания числа СН 3
в частице углеводорода, точка кипения его падает. Удельный вес П. растет
сравнительно медленно; замечательно, что, начиная с С 11 Н 24
и дальше, уд. вес углеводородов, определенный при темп. их плавл., является
почти постоянной величиной. В табл. в 1-м столбце стоит формула П., во 2-м его
название и фамилия автора, определившего приводимые свойства, в 3-м точки
плавления, в 4-м точки кипения и в 5-м удельные веса
|
СH 4 |
Метан (Вроблевский,
Ольшевский) |
—186° |
—164° |
0,415 (—161°) |
|
С 2 Н 6 |
Этан |
газы: физические
постоянные |
|
|
|
С 3H8 |
Пропан |
не определены. |
|
|
|
С 4 Н 10 |
Бутан (Бутлеров) |
— |
+1° |
— |
| |
Метилпропан (Бутлеров) |
— |
— 17° |
— |
| C5H12 |
Пентан (Шорлеммер) |
— |
+37° |
0,627 (14°) |
| |
Диметилпропан (Львов) |
—20° |
+9° |
— |
|
С 6 Н 14 |
Гексан (Шифф, Брюль,
Цандер) |
— |
69° |
0,658 (20°) |
| |
Диметил-2-бутан
(Горяинов) |
— |
48° |
— |
|
С 7 Н 16 |
Гептан (Торпе,
Шорлеммер) |
— |
98° |
0,683 (20°) |
|
С 8 Н 18 |
Октан (Торпе) |
— |
125° |
0,702 (20°) |
|
С 9 Н 20 |
Нонан (Крафт) |
—51° |
150° |
0,718 (20°) |
|
С 10 Н 22 |
Декан (Крафт) |
—31° |
173° |
0,730 (20°) |
|
С 11 Н 24 |
Гендекан [Чаще С 11 Н 24
называется ундеканом] (Крафт) |
—26° |
195° |
0,774 (— 26°) |
|
С 12 Н 26 |
Додекан (Крафт) |
—12° |
214° |
0,773 (— 12°) |
|
С 13 Н 28 |
Тридекан (Крафт, Май) |
—6° |
234° |
0,775 (— 6°) |
|
С 14 Н 30 |
Тетрадекан (Крафт) |
+4° |
252° |
0,775 (+4°) |
|
С 15 Н 32 |
Пентадекан (Крафт,
Май) |
+10° |
270° |
0,776 (+10°) |
| C20H42 |
Эйкозан (Крафт) |
37° |
205° (15 мм) |
0,778 (37°) |
|
С 21 Н 44 |
Генэйкозан (Крафт) |
40° |
215° (15 мм) |
0,778 (40°) |
|
С 22 Н 46 |
Докозан (Крафт) |
44° |
224° (15 мм) |
0,778 (44°) |
|
С 23 Н 48 |
Трикозан (Крафт) |
48° |
234° (15 мм) |
0,779 (48°) |
|
С 35 Н 72 |
Пентатриаконтан
(Крафт) |
75° |
331° (15 мм) |
0,782 (75°) |
|
С 60 Н 122 |
Гексаконтан (Гелль и
Гегеле) |
101° — 102° |
— |
— |
Если отнести точки плавления нормальных П. к прямоугольным осям, принимая их
за ординаты, а за абсциссы число атомов углерода в частицах, то получаются две
гиперболических кривых; вышележащая обнимает собой точки плавления П. с четным
числом атомов углерода, а нижележащая отвечает точкам плавления П. с нечетным
числом атомов С [Подобная же правильность давно установлена Байером для точек
плавления двухосновных предельных жирных кислот и в 1896 г. Массолем для точек
плавления одноосновных предельных, нормальных жирных кислот.]. На точках кипения
их можно подметить такую же правильность (Милльс), хотя и менее резко
выраженную. Что касается малой изменяемости удельных весов высших П., то она
равносильна прямолинейной зависимости их удельных объемов от частичного веса.
Все П. бесцветны, мало растворимы в воде; средние члены недурно растворимы в
спирте и хорошо в эфире; высшие члены и в последнем трудно растворимы.
В химическом отношении П. характеризуются значительной индифферентностью; на
холоде на них почти не действуют: крепкая серная кислота, крепкая азотная (ср.
ниже образование нитросоединений), смесь обеих кислот, хромовая кислота и
некоторые другие, так наз. "энергичные" реактивы. Впервые эти свойства были
наблюдены в 1830 г. Рейхенбахом, выделившим смесь высших, твердых П. из
продуктов сухой перегонки
дерева, а потому он и дал ей название (считая добытое вещество однородным)
"paraffin" (от лат. слов par um
и аffinis), чтобы характеризовать "ее главное свойство, заключающееся в
незначительности ее сродств"; впоследствии, когда стали известны низшие члены
ряда, название П. было перенесено и на них Г. Уатсом. При нагревании крепкая
азотная кислота и другие энергичные окислители разрушают П., образуя в конце
концов углекислоту и воду; побочными продуктами в небольшом количестве являются
жирные кислоты, янтарные кисл. и некоторые другие окисленные вещества (см.).
Слабая азотная кислота (уд. в. 1,036—1,075 при 120° — 140°) нитрует П., образуя
нитросоединения (М. Коновалов, XXI, 198). Хлор действует на П. под влиянием
рассеянного света уже на холоде, образуя продукты замещения (см. Хлоропарафины);
на прямом солнечном свете реакция метана с хлором может дойти до взрыва и
продуктами ее являются уголь и хлористый водород: mСН 4
+ 2mСl 2 = mC +
4mНСl; замещение водорода хлором в П. идет легко в присутствии небольшого
количества йода и при нагревании; для СН 4, C2H6
и C 3H8
получены, кроме промежуточных, и продукты полного замещения водорода хлором, т.
е. ССl 4, C2 Сl 6
и C 3 Сl 8;
начиная с C 4H10
наблюдается при энергичном хлорировании распадение углеводорода (ср. выше об
отношении П. к нагреванию их с АlСl 3)
и продуктами его являются CCl 4, C2Cl6, C4Cl6
и C 6Cl6
(гексахлорбензол; Крафт и Мерц). До 1848 г. из П. был известен почти только один
метан CH 4; в этом
году Кольбе и Франкланд открыли образование П. (ср. выше) при электролизе солей
жирных кислот и нагревании йодюров спиртов с цинком; полученные таким образом
углеводороды были приняты за настоящие радикалы (см.) спиртов и этан С 2 Н 6
получил название метила-СН 3
и т. д. Жерар тогда же, руководствуясь законом Авогадро (см. Частичная
гипотеза), высказался за удвоение их формул и за то, что открытые углеводороды
являются гомологами (см. Гомология) метана; к тому же склонился и Гофман,
опиравшийся на правильности в точках кипения гомологов, установленных ранее
Коппом (см. Температуры
кипения органич. соединений). Кроме "радикалов" Франкландом были еще получены
углеводороды ряда С n Н 2n+2,
которые он считал полимерными с первыми и, принимая их за настоящие гомологи СН 4,
назвал водородистыми радикалами; таким образом принималось существование CH 3 '
— радикала метила и С 2 Н 5 (H)
— водородистого этила. Тождество обоих рядов было установлено изучением их
продуктов замещения. Бертело показал, что СН 3 Сl
продукт замещения хлором 1 ат. водорода метана тождествен с хлористым метилом,
получаемым из метилового спирта действием соляной кислоты: CH 3(OH)
+ HCl = CH3Cl + H2 O;
затем целый ряд монохлоропродуктов П. и водородистых радикалов был изучен
Шорлеммером, показавшим
их полное тождество; в особенности
решающее значение имело наблюдение, что как из "метила", так и из водородистого
этила получается один и тот же хлористый этил C 2H5 Cl
(Шорлеммер), переходящий при нагревании с водой в винный спирт (Бутлеров); почти
одновременно (годом раньше) было установлено, что "этил" C 2H5 '
Франкланда при действии хлора дает хлористый бутил — С 4 Н 9 Сl
(Шейен). О тождестве хлористого метила см. Хлористый метилен).
Все П. делятся по строению на нормальные общей формулы: СН 3 —(СH 2)n —СН 3
и остальные, содержащие больше метильных групп и для которых нет общепринятых
классов [По Роско и Шорлеммеру, остальные П. делятся на "изо" П. — с тремя
метиловыми группами, "мезо" П. напр. (СН 3)2 CH—CH(СН 3)2
и (СН 3)2 СН—СН(СН 3)—СН 2 —СH(CH 3)2
и "нео" П. — напр. С(СН 3)4
и т. д. Эта классификация не получила права гражданства.].
Число возможных изомеров с нарастанием числа атомов С в частице быстро
увеличивается, как видно из следующей таблички (Кейлей, Германн):
|
Число атомов С |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 и т. д. |
|
" возм. изомеров |
1 |
1 |
1 |
2 |
3 |
5 |
9 |
18 |
35 |
75 |
159 |
355 |
802 и т. д. |
Надо заметить, что при составлении этой таблицы не принята во внимание
"оптическая" ("геометрическая", см. Стереохимия) изомерия П., а она несомненно
возможна, как видно из того, что несколько оптически деятельных П. теперь уже
известны, напр. CH 3—CH(C2H5)—СН 2 —СH 2 —СН 3,
для которого [α] = +3,93° (Юст), СН 3 —СН(С 2 Н 5)—СН 2 —СH 2 —СН(С 2H5)—СН 3
с [α] = +8,69° (Юст) и т. д.; если же принять во внимание возможность оптически
деятельных П. и вероятность их "рацемических" (см. Винная кисл.) форм, то число
возможных изомеров должно еще возрасти. В сравнении с этими громадными числами
количество известных П. ничтожно.
В заключение несколько слов о современной номенклатуре П., выработанной
женевским конгрессом 1892 г. Названия всех П., как давно предложено Гофманом,
оканчиваются слогом "ан" и для "нормальных" П. они следующие: метан — СН 4,
этан — С 2 Н 6,
пропан — С 3 Н 8,
бутан — C 4H10;
начиная с C 5H12,
название составляется из греч. числительного и слога "ан", напр. C 5H12
— пентан, C 6H14
— гексан и т. д. (см. выше табл.). П. не нормального строения рассматриваются
как продукты замещения нормальных, остатками каковых считаются наиболее длинные
углеродные цепи; напр.
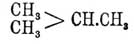 есть
метилпропан (ранее был назван Бутлеровым изобутаном), а есть
метилпропан (ранее был назван Бутлеровым изобутаном), а
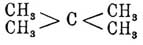 —
диметилпропан (тетраметилформен Львова). Когда замещающая группа находится в
боковой цепи, то вместо метила, этила и т. д. говорят мето-, это- и так далее,
например —
диметилпропан (тетраметилформен Львова). Когда замещающая группа находится в
боковой цепи, то вместо метила, этила и т. д. говорят мето-, это- и так далее,
например 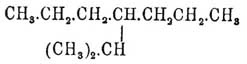 есть метоэтилгептан. Положение боковой цепи указывается цифрой, которой
обозначен углеродный атом главной цепи, причем счет ведется с конца более
близкого к наиболее простой замещающей группе; напр.
есть метоэтилгептан. Положение боковой цепи указывается цифрой, которой
обозначен углеродный атом главной цепи, причем счет ведется с конца более
близкого к наиболее простой замещающей группе; напр.
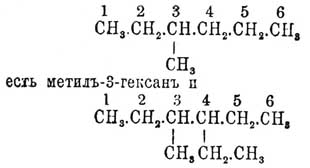 есть
метил-3-гексан, и есть
метил-3-гексан, и
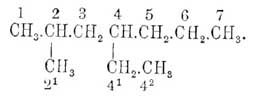 есть
метил-3-этил-4-гексан. Углеродные атомы боковых цепей обозначаются цифрой
углеродного атома главной цепи, к которой он примыкает; эта цифра снабжается
показателем, напр. есть
метил-3-этил-4-гексан. Углеродные атомы боковых цепей обозначаются цифрой
углеродного атома главной цепи, к которой он примыкает; эта цифра снабжается
показателем, напр.
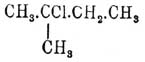 . .
Когда с одним углеродным атомом соединены две замещающих группы, то
простейшая называется первой; напр.
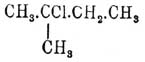 есть
2-метил-2-хлорбутан. есть
2-метил-2-хлорбутан.
А. И. Горбов. Δ.
|