Окись этилена
(oxyde d'éthylène, ä thylenoxyd,
хим.) 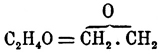 —
получена впервые Вюрцем при действии концентрированного раствора едкого кали на
хлоргидрин гликоля (см.): СlН 2 С.CН 2 (ОН)
— HCl = (CH 2)2 O;
удобнее получается она из хлорацетина гликоля [Хлорацетин гликоля получается
(Симпсон) при насыщении хлористым водородом моноацетина (HO)H 2 С.CН 2.О 2 С.CН 3
+ НСl = СlН 2 С.CН 2.О 2 С.CН 3,
а моноацетин образуется при кипячении с обратно поставленным холодильником
бромистого этилена (1
часть) с уксуснокалиевой солью (1
часть) и 85% спиртом (2 части; Аткинсон): —
получена впервые Вюрцем при действии концентрированного раствора едкого кали на
хлоргидрин гликоля (см.): СlН 2 С.CН 2 (ОН)
— HCl = (CH 2)2 O;
удобнее получается она из хлорацетина гликоля [Хлорацетин гликоля получается
(Симпсон) при насыщении хлористым водородом моноацетина (HO)H 2 С.CН 2.О 2 С.CН 3
+ НСl = СlН 2 С.CН 2.О 2 С.CН 3,
а моноацетин образуется при кипячении с обратно поставленным холодильником
бромистого этилена (1
часть) с уксуснокалиевой солью (1
часть) и 85% спиртом (2 части; Аткинсон):
BrH2 C.СН 2Br
| KO2C.CH3 + C2H6 O
= (НО)H 2 С.CН 2 (О 2 С.CН 3
+ KBr + ВrС 2 Н 5.];
ClH2C.CH2(OOC.CH3)
+ 2KОН = (СН 2)2 О
+ KCl + KООС.CH 3 + H2 O
(Демоль);
в том и другом случае продукт реакции, газообразный при обыкновенной
температуре, пропускают для осушения через трубку с хлористым кальцием и
собирают в приемнике, охлажденном смесью льда со снегом. О. этилена образуется
еще при нагревании с О. серебра йодистого (при 150°) или бромистого этилена (при
250°): С 2H4I2 + Ag2 О
= (С 2 Н 4)"О
+ 2AgI и О. натрия с бромистым этиленом (при 180°): С 2 Н 4Br2
+ Na2O = (C2H4)"O
+ 2NaBr (? Грин). О. этилена представляет прозрачную, легкоподвижную жидкость,
обладающую приятным, отчасти эфирным запахом, кипит при 14°; удельн. вес (при
0°) = 0,8963 (Вюрц); с водой О. этилена смешивается во всех отношениях; водный
раствор восстановляет аммиачную О. серебра, но труднее, чем раствор
обыкновенного альдегида (с которым О. этилена изомерна), и под влиянием
платиновой черни образует гликолевую кислоту: С 2H4 О
+ О 2 = СН 2 (ОН).COOH
[Может быть, первоначально О. этилена переходит, присоединяя элементы воды, в
гликоль.]. При нагревании (в запаянных трубках) с водой О. этилена соединяется с
нею, давая обратно гликоль, при избытке воды, или полиэтиленовые алкоголи (см.),
при недостатке Н 2 О
(см.). При действии пятихлористого фосфора О. этилена дает хлористый этилен: (СН 2 СH 2)"О
+ РСl 5 = СlН 2 С.CН 2 Сl
+ РОСl 3. Наиболее
характерны для О. этилена реакции присоединения. Так, она легко соединяется (при
действии амальгамы натрия) с водородом, образуя спирт обыкновенный: (С 2 Н 4)"О
+ Н 2 = C2H5 (OH)
(Вюрц). Газообразная О. этилена с большой энергией соединяется с газообразным
хлористым водородом, образуя обратно хлоргидрин гликоля: (С 2 Н 4)"О
+ НСl = С 2 Н 4 Сl(ОН);
реакция идет легко и в водных растворах, даже при действии О. этилена на водные
растворы хлористых металлов, причем образуются гидраты их О., например: 2(C 2H4)"O
+ MgCl3 + 2H2O = 2C2H4Cl(OH) +
Mg(OH)2, которые и
осаждаются (кроме Mg(OH), могут быть осаждены О. этилена — Al(OH) 3,
Fe(OH)3 и Cu(ОН) 2;
Вюрц). Реагируя с синильной кислотой O. этилена образует нитрил этиленмолочной
(см. Гидракриловая кислота) кислоты: (С 2 Н 4)"О
+ HCN = (HO)CH 2.CH2.CN
(Вюрц). С аммиаком О. этилена реагирует очень легко (Вюрц) и если действовать на
избыток аммиака (при сильном охлаждении), то затем фракционировкой удается
выделить амидоэтиловый (этаноламин) спирт: (С 2 Н 4)"О
+ NH 3 = H2N.C2H4 (OH),
диэтаноламин HO.C 2H4.NH.C2H4.OH
= 2(C2H4)"O + NH3
и триэтаноламин (HO.C 2H4)3N = 3(C2H4)"O
+ NH3 (Кнорр). С
концентрированным водным раствором триметиламина окись этилена образует холин:
(CH3)3N + C2H4 O
+ Н 2 О = НО.N(CH 3)3.СН 2.СH 2.ОН
(Вюрц).
А. И. Горбов. Δ .
|