Изомерия
(хим.). — В 1824 г. Либихом и Гей-Люссаком был установлен состав
гремучекислого серебра (см.), при чем, на основании полученных данных, они
признали безводную [Согласно господствовавшему в химии в начале нынешнего
столетия взгляду, кислотами считались
современные ангидриды их (см.
Дуализм и Кислоты). Состав безводной кислоты выводился из данных анализа солей
(в описываемом случае серебряной и ртутной), при чем считалось, что металл (в
кислородных солях) входит в состав соли в виде окиси.] гремучую кислоту за
соединение циана с кислородом С 4N2O2
(С = 6, О = 8, N = 14). В том же году Веллер более точными анализами солей
циановой кислоты, открытой им в 1822 г., показал, что и безводная циановая
кислота, по элементарному составу, представляет соединение циана с кислородом, C 2 NO
(С = 6, О = 8, N = 14). Таким образом, впервые были получены вещества одного и
того же элементарного и процентного состава, но различных свойств (соли гремучей
кислоты взрывают с большой энергией от легкого толчка, между тем как соли
циановой кислоты совершенно лишены этой способности). Хотя Гей-Люссак, реферируя
в "Annales de chimie et de phisique" (27, [2], 200) работу Веллера, и указал на
возможность объяснения этого явления допущением различного способа соединения
между элементами, образующими гремучую и циановую кислоты, тем не менее оно
настолько противоречило существовавшему в то время в химии положению, что
свойства тел обусловливаются их элементарным и процентным составом, что
Берцелиус, не колеблясь (в появившемся тогда новом издании своего "Trait é
de Chimie"), объявил, что в данные Гей-Люссака и Либиха или Веллера вкрались
ошибки; понадобились новые анализы, произведенные Либихом в 1826 г., чтобы
доказать тожество состава гремучих и циановых солей. К 1826 г., впрочем, было
уже известно другое, вполне аналогичное явление. Фарадей в 1825 г., исследуя
жидкость, скопившуюся в цилиндрах, в которых сохранялся сдавленный светильный
газ, нашел в ней, вместе с бензолом (см.), вещество (см. Бутилен) С 4 Н 8
одинакового состава с
этиленом С 2 Н 4,
но обладавшее удвоенной сравнительно с последним плотностью пара. Затем, в 1828
г., Веллеру удалось наблюсти, что циановокислый аммоний CNO.NH 4
(С = 12, 0 = 16, N = 14, H = 1) нацело превращается в водных растворах в
мочевину (см.) CO(NH2)2,
и, наконец, в 1830 г. Берцелиус, исследуя виноградную кислоту (см.), нашел, что
как сама свободная кислота, так и ее свинцовая соль обладают одинаковым
процентным составом с винной кислотой и виннокислым свинцом, между тем как
свойства и свободных кислот и их солей довольно сильно различаются между собою
(см. Винная кислота). Этими наблюдениями окончательно была установлена
возможность существования различных по свойствам, но тожественных по
элементарному и процентному составу, химических соединений, и в отчете по химии,
представленном Шведской академии наук в 1831 г., Берцелиус замечает по этому
поводу, что "так как необходимо для каждого известного представления обладать
определенным выражением, выбранным по возможности рационально, то я предлагаю
называть тела одного состава, но различных свойств, изомерными (от греческого
слова ίσομερής — составленный из равных частей)". Уже в следующем году он дает
более ограниченное определение нового понятия. "Чтобы не смешать, однако, друг с
другом явления не вполне однородные", говорит он, "необходимо точно установить
значение слова — И. Я считаю изомерными те тела, которые образованы из
одинаковых атомов, соединенных в одинаковых относительных и абсолютных
количествах, которые обладают одинаковым весом атома [Частичным весом
современной химии.]. С этим случаем нельзя смешивать того, когда в двух телах
содержатся одинаковые относительные количества элементарных тел, при разном
абсолютном содержании этих последних. Так, напр., относительное число атомов
углерода и водорода в маслородном газе (этилене) и в винном масле (бутилене)
тожественно, но в одном из них содержится только один атом углерода, 2 атома
водорода СН 2,
между тем как в винном масле находятся 4 атома углерода и 8 атомов водорода С 4 Н 8
[Верные формулы: этилена — С 2 Н 4
и бутилена — С 4 Н 8
(С = 12, Н = 1).]. Для отличия подобных случаев одинаковости состава при
различии в других свойствах, я предложил бы называть их полимерными (от греч.
πολλύς — множественный и μέρος — часть)... Но существуют и другие отношения, при
которых тела, по-видимому изомерные в строгом смысле этого слова, т. е.
содержащие одинаковые элементы и абсолютно тожественные количества атомов, на
самом деле не являются таковыми. Подобные случаи наблюдаются для тел,
образованных соединением двух атомов [Под словом атом и здесь надо понимать
частицу химического соединения.] первого порядка; напр. SnO.SO 3
— сернокислая закись олова, и
SnO 2.SO2
— основная сернисто-кислая соль
окиси олова, содержат одинаковые абсолютные и относительные количества атомов
одних и тех же элементов, имеют одну и туже частицу, а между тем их нельзя
считать за одно вещество. В таких телах с течением времени, или с изменением
темпер., происходит обыкновенно перемещение их составных частей [Под словами
"составные части" подразумеваются окислы серы и олова, которые, по Берцелиусу,
существовали в описываемых соединениях как таковые. Упоминаемое превращение
очень поучительно и для господствующих воззрений (см. Унитарное учение).],
иногда сопровождаемое повышением темпер.,
вследствие чего образуются новые соединения. Чтобы резко отличить эти случаи от
явлений И., можно подобные тела назвать метамерными (употребляя предлог μετά с
тем же значением, которое он имеет в слове метаморфоза)". С тех пор, с развитием
органической химии [Между неорганическими веществами известно очень немного
изомерных веществ, и они не играли никакой роли в выработке понятия об И. Их и
теперь тем удобнее оставить в стороне, что твердо установлена величина частиц
слишком малого числа неорганических веществ.], фактические сведения о телах,
обладающих различными свойствами при тожественном составе, чрезвычайно возросли
(так, напр., в 1884 г. В. Мейер насчитал 55 различных соединений, отвечающих
общей формуле С 9 Н 10 О 3,
а в течение 10 лет это число значительно увеличилось), но нельзя сказать, чтобы
понятия, введенные в химию Берцелиусом, выиграли в ясности и определенности.
Впрочем, надо заметить, что и те примеры, на основании которых были установлены
эти понятия, оказались неудачно выбранными; теперь мы знаем, что виноградная
кислота обладает удвоенною частицей сравнительно с обыкновенной винною кислотою
(см.), но что кроме того ее нельзя рассматривать как полимерную винную кислоту
потому, что она образована соединением оптически противоположных, правой и
левой винных кислот. Циановая
кислота и гремучая кислота обладают тоже различной величиной частиц, при
различном строении, а циановокислый аммоний и мочевина представляют тела
различных функций и, по современным структурным представлениям, содержат
различные группы атомов (различные остатки), а именно строение 1-го выражается
формулой N:C-O.NH4,
а второй — формулой NH 2.CO.NH2.
Изомерными теперь называют вообще все тела одного и того же процентного состава
и одной и той же частичной формулы и отличают: 1) изомеры собственно,
когда при одной и той же частичной формуле вещества обладают однородной
химической функцией [Так, например, изомерными считаются бутиловые спирты,
отвечающие формуле C 4H10 O,
именно: CH 3.CH2.CH2.CH2 (OH)
— нормальный бутиловый спирт, CH 3.CH2.CH(OH)CH3
- вторичный
бутиловый спирт, (CH 3)2:CH.CH2 (OH)
— изобутиловый спирт и (CH3)3:C(OH)
— третичный бутиловый спирт
(триметилкарбинол).]; изомеры случайные, когда при одной и той же
частичной формуле они обладают различной химической функцией [Примерами
случайной изомерии с упомянутыми (см. пред. прим.) бутиловыми спиртами могут
служить: C 2H5O.C2H5 -
обыкновенный или серный эфир,
CH 3O.C3H7
— метилпропиловый и
метиловопропиловый эфир; формуле C 3H6 O
отвечают случайные изомеры: аллиловый спирт — CH 2:CH.CH2 (OH),
ацентон — CH 3.CO.CH3,
окись пропилена
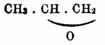 ,
окись триметилена — ,
окись триметилена —
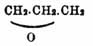 , пропионовый
альдегид — CH 2.CH2.CHО
и т. д.] и 3) метамеры — вещества, обладающие одной и той же частичной
формулой, одной и той же химической функцией, но (как выражаются иногда)
нецельной частицей [Метамерны между собою упомянутые выше простые эфиры (см.
пред. прим.) или же, напр., CH 3.O2C2H3
— уксусно-метиловый эфир и C 2H5.O2CH5
— муравьино-этиловый, оба
отвечающие формуле C 3H6O2
и оба случайно изомерные с пропионовой кислотою: CH 3.CH2.COOH.].
Вещества, обладающие при одинаковом процентном составе различными частичными
формулами, т. е. полимерные между собой, не причисляются более к изомерам (см.
Полимерия). Такое деление, однако, далеко не общепринятое. Очень часто, напр.,
спирты и эфиры одной с ними частичной формулы (см. прим.) назыв. метамерными
соединениями (Бернтсен); в руководстве Бейльштейна "Handbuch der Org. Chemie"
(3-te Aufl. S. 5): изомерами, в тесном смысле этого слова, согласно определению
Бутлерова и Клауса, сочтены только соединения, в которых углеродные атомы
связаны одинаково, а другие элементы сгруппированы различным образом, каковы: СН 3.СН 2.СН 2 (ОН)
— пропиловый спирт и СН 3.СН(ОН).СН 3
— изопропиловый спирт;
метамерными же названы соединения, в которых углеродные атомы связаны различным
образом, а тожественно сгруппированы остальные, соединенные с углеродом
элементы, и как примеры приведены СН 3.СН 2.СН 2.СН 2 (ОН)
— нормальный бутиловый и (СН 3)2:СН.СН 2 (ОН)
— изобутиловый спирты; наконец, изометамерными названы изомеры, в которых и
углеродные атомы, и атомы остальных элементов связаны различным образом, как,
напр., в нормальном бутиловом спирте — СН 3.СН 2.СН 2.СН 2 (ОН)
и в триметилкарбиноле — (CH3)3:C(OH).
Неудобство такого определения
совершенно ясно; приняв его, мы должны признать, что между углеводородами
возможны только случаи метамерии и изометамерии, а это совершенно несогласно с
установившимся обычаем. Можно было бы привести еще несколько аналогичных
примеров не менее произвольных определений (и основанных на них классификаций);
достаточно, однако, и перечисленных, чтобы видеть, что значения, приобретенные
словами: И. и метамерия, значительно уклонились от того смысла, который им
придавал Берцелиус и который они должны иметь по самому словопроизводству.
Строго говоря, раз, по современным воззрениям, мы допускаем возможность знать
ближайшее распределение элементов в частицах данного вещества — его "структуру"
(см. Строение хим. и Стереохимия), то изомерами, в органической химии, по
крайней мере, можно называть только те тела, структурные формулы которых
содержат одни и те же группы атомов, т. е. тожественные остатки: СН 3,СН" 2,
СН"', СО", (СОН)', (СООН)', (ОН)',О" и т. д.; метамерными же, в смысле
Берцелиуса, можно называть только тела, способные к превращению друг в друга с
сохранением одной и той же величины частицы. При таком определении, изомерами из
числа бутиловых спиртов (см.), напр., являлись бы только (СН 3)2:СН.СН 2 (ОН)
— изобутиловый спирт, и СН 3.СН 2.СН(ОН).СН 3
— псевдобутиловый
(вторичнобутиловый) спирт, метамерами же, если ограничиться уже приведенными
примерами — циановокислый аммоний и мочевина. Для огромного, однако, числа
веществ, теперь причисляемых к изомерным, не было бы соответственного названия,
и потому заслуживают большего внимания следующие предложения Армстронга. Он
предлагает называть все случаи различия свойств веществ, при тожестве их
состава, не И., а аллотропией (от греческого άλλότροπος, что значит — обладающий
отличными свойствами [Слово аллотропия предложено в 1841 г. Берцелиусом для
характеристики различных (по физическим и химическим свойствам) видоизменений
элементарных тел, каковы, напр., различные видоизменения серы. (см.), фосфора
(см.) и т. д. В том смысле, в котором предлагает его употреблять Армстронг, оно
довольно близко подходит, по содержанию, к слову "аллоизомерия" (от греч. άλλος—
другой и ίσομερής), предложенному Михаэлем, для отличия тех случаев различия в
свойствах тожественных по составу органических соединений, когда, по большинству
наблюденных превращений, им приходится придавать одну и ту же структурную
формулу (подробнее см. Стереохимия)], слово же И. употреблять в том тесном
смысле, который только что изложен, включая следовательно сюда и все явления
пространственной И. (см. Стереохимия), вещества же аллотропичные (изомерные), но
различные по функции или по типу, к которому они принадлежат, Армстронг называет
гетерометричными [От ητέρος — другой и μέτρον — мера.], оставляя название
метамерных или изодинамичных [От ίσος — равный и δύναμις— сила.]
для тех из них, которые превращаются друг в друга с исключительной легкостью.
Все же остальные случаи, где аллотропичные вещества обладают одной и той же
функцией, но образованы соединением нетожественных групп, он считает возможным
называть изономичными [От ίσος и
νόμος — закон.] (см. Кеномерия,
Меротропия и Таутометрия). , пропионовый
альдегид — CH 2.CH2.CHО
и т. д.] и 3) метамеры — вещества, обладающие одной и той же частичной
формулой, одной и той же химической функцией, но (как выражаются иногда)
нецельной частицей [Метамерны между собою упомянутые выше простые эфиры (см.
пред. прим.) или же, напр., CH 3.O2C2H3
— уксусно-метиловый эфир и C 2H5.O2CH5
— муравьино-этиловый, оба
отвечающие формуле C 3H6O2
и оба случайно изомерные с пропионовой кислотою: CH 3.CH2.COOH.].
Вещества, обладающие при одинаковом процентном составе различными частичными
формулами, т. е. полимерные между собой, не причисляются более к изомерам (см.
Полимерия). Такое деление, однако, далеко не общепринятое. Очень часто, напр.,
спирты и эфиры одной с ними частичной формулы (см. прим.) назыв. метамерными
соединениями (Бернтсен); в руководстве Бейльштейна "Handbuch der Org. Chemie"
(3-te Aufl. S. 5): изомерами, в тесном смысле этого слова, согласно определению
Бутлерова и Клауса, сочтены только соединения, в которых углеродные атомы
связаны одинаково, а другие элементы сгруппированы различным образом, каковы: СН 3.СН 2.СН 2 (ОН)
— пропиловый спирт и СН 3.СН(ОН).СН 3
— изопропиловый спирт;
метамерными же названы соединения, в которых углеродные атомы связаны различным
образом, а тожественно сгруппированы остальные, соединенные с углеродом
элементы, и как примеры приведены СН 3.СН 2.СН 2.СН 2 (ОН)
— нормальный бутиловый и (СН 3)2:СН.СН 2 (ОН)
— изобутиловый спирты; наконец, изометамерными названы изомеры, в которых и
углеродные атомы, и атомы остальных элементов связаны различным образом, как,
напр., в нормальном бутиловом спирте — СН 3.СН 2.СН 2.СН 2 (ОН)
и в триметилкарбиноле — (CH3)3:C(OH).
Неудобство такого определения
совершенно ясно; приняв его, мы должны признать, что между углеводородами
возможны только случаи метамерии и изометамерии, а это совершенно несогласно с
установившимся обычаем. Можно было бы привести еще несколько аналогичных
примеров не менее произвольных определений (и основанных на них классификаций);
достаточно, однако, и перечисленных, чтобы видеть, что значения, приобретенные
словами: И. и метамерия, значительно уклонились от того смысла, который им
придавал Берцелиус и который они должны иметь по самому словопроизводству.
Строго говоря, раз, по современным воззрениям, мы допускаем возможность знать
ближайшее распределение элементов в частицах данного вещества — его "структуру"
(см. Строение хим. и Стереохимия), то изомерами, в органической химии, по
крайней мере, можно называть только те тела, структурные формулы которых
содержат одни и те же группы атомов, т. е. тожественные остатки: СН 3,СН" 2,
СН"', СО", (СОН)', (СООН)', (ОН)',О" и т. д.; метамерными же, в смысле
Берцелиуса, можно называть только тела, способные к превращению друг в друга с
сохранением одной и той же величины частицы. При таком определении, изомерами из
числа бутиловых спиртов (см.), напр., являлись бы только (СН 3)2:СН.СН 2 (ОН)
— изобутиловый спирт, и СН 3.СН 2.СН(ОН).СН 3
— псевдобутиловый
(вторичнобутиловый) спирт, метамерами же, если ограничиться уже приведенными
примерами — циановокислый аммоний и мочевина. Для огромного, однако, числа
веществ, теперь причисляемых к изомерным, не было бы соответственного названия,
и потому заслуживают большего внимания следующие предложения Армстронга. Он
предлагает называть все случаи различия свойств веществ, при тожестве их
состава, не И., а аллотропией (от греческого άλλότροπος, что значит — обладающий
отличными свойствами [Слово аллотропия предложено в 1841 г. Берцелиусом для
характеристики различных (по физическим и химическим свойствам) видоизменений
элементарных тел, каковы, напр., различные видоизменения серы. (см.), фосфора
(см.) и т. д. В том смысле, в котором предлагает его употреблять Армстронг, оно
довольно близко подходит, по содержанию, к слову "аллоизомерия" (от греч. άλλος—
другой и ίσομερής), предложенному Михаэлем, для отличия тех случаев различия в
свойствах тожественных по составу органических соединений, когда, по большинству
наблюденных превращений, им приходится придавать одну и ту же структурную
формулу (подробнее см. Стереохимия)], слово же И. употреблять в том тесном
смысле, который только что изложен, включая следовательно сюда и все явления
пространственной И. (см. Стереохимия), вещества же аллотропичные (изомерные), но
различные по функции или по типу, к которому они принадлежат, Армстронг называет
гетерометричными [От ητέρος — другой и μέτρον — мера.], оставляя название
метамерных или изодинамичных [От ίσος — равный и δύναμις— сила.]
для тех из них, которые превращаются друг в друга с исключительной легкостью.
Все же остальные случаи, где аллотропичные вещества обладают одной и той же
функцией, но образованы соединением нетожественных групп, он считает возможным
называть изономичными [От ίσος и
νόμος — закон.] (см. Кеномерия,
Меротропия и Таутометрия).
А. И. Горбов.
Δ .
|