Эритрит
(хим.) — бутантетрол С 4 Н 6 (ОН) 4
= (HО)Н 2 С.СН(ОН).СН(ОН).СH 2 (ОН)
— четырехатомный предельный спирт, содержащий два асимметричных атома углерода
(напечатаны курсивом), а потому возможный, подобно винной кислоте (см. и ср.
Стереоизомерия), в четырех видоизменениях: двух оптически деятельных (право- и
левовращающих), одном — рацемическом и одном — мезотипа; все четыре известны.
Правый — d.-Э. (ср. Гидраты углерода) получен Г. Бертраном; исходным
веществом является мезоэритрит (см. ниже), который окисляют в эритрулозу,
культивируя в его 4 %-м водном растворе сорбозебактерию:
(HO)H2C.CH(OH).CH(OH).CH2(OH) + O" = H2 O
+ (НО)Н 2 С.СО.СН(ОН).СН 2 (ОН)
(эритрулоза);
кетоноспирт восстановляют затем в слабокислой среде амальгамой натрия; из
сиропа, остающегося после удаления неорганических солей, выделяют
регенерированный мезоэритрит кристаллизацией с помощью готового кристаллика, а
d.-Э. очищают, переходя через трудно растворимый дибензацеталь — С 4 Н 6 О 4 (С 7 Н 6)2.
Из воды, в которой он очень хорошо растворим, d.-Э. кристаллизуется, имея
плоскости гексагональной призмы и простого ромбоэдра, без признаков гемиэдрии
(Вырубов); он плавится при 88—89° Ц.; [α ]D
= —4°46'; трудно растворим в кипящем спирте; при нагревании на водяной бане с
тройным по весу количеством HNO 3
(d—1,2) до сиропообразной консистенции дает правую (обыкновенную) винную кислоту
(Бертран и Макэн), чем объясняется и название Э., как правого (ср. Гидраты
углерода, прим.). Описаны многие производные этого Э.
Левый l.-Э. получен Макэном из l.-ксилозы (см. Гидраты углерода и
Глюкозы, l. с.) методом Воля, для чего ксилозу действием концентрированного
спиртового раствора гидроксиламина (см.) переводят в ксилозоксим: С 5 Н 10O5
+ (НО)Н 2 N = Н 2 О
+ С 5H11 О 5 N,
— нагреванием с уксусным ангидридом и уксусно-натриевой солью его ацетилируют и,
отнимая воду, превращают в l.-ацетилксилонитрил (ср. Изонитрозосоединения), а
затем, отщепляя от последнего элементы HCN и обмыливая, получают l.-эритрозу
(альдегид l.-Э.), которую и восстанавливают амальгамой натрия в слабокислом
растворе в l.-Э. Физические свойства последнего повторяют буквально свойства
d.-Э. (Вырубов, Макэн); вращение равно по величине, но противоположного знака
(правое). При окислении азотной кислотой (условия выше) l.-Э. образует левую
винную кислоту (Бертран и Макэн).
Рацемический Э. получен впервые Гринером, путем довольно сложных
превращений, а именно: дивинил (см. Винилэтилен, Углеводороды ацетиленовые),
синтезированный, между прочим, Бертело из ацетилена и этилена, превращают
сначала осторожным действием брома в малопостоянный дибромид, дающий выше 100°
два стереоизомера:
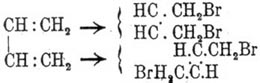 , из которых
один BrH 2 C.СН:СН.СН 2 Br,
жидкий при обыкновенной температуре, кипящий при 70° (20 мм) и образующийся в
незначительном количестве, дает при окислении слабым раствором
марганцево-калиевой соли на холоде дибромгидрин мезоэритрита BrH 2 C.СН(ОН).СН(ОН).CH 2 Br,
плавящийся при 135°; а второй — Br 2C.CH=CH.CH2 Br
— кристаллический, плавящийся при 53—54°, кипящий при 92—93° (15 мм), являющийся
главным продуктом превращения, образует при окислении KMnO 4
дибромгидрин рацемичного Э. , из которых
один BrH 2 C.СН:СН.СН 2 Br,
жидкий при обыкновенной температуре, кипящий при 70° (20 мм) и образующийся в
незначительном количестве, дает при окислении слабым раствором
марганцево-калиевой соли на холоде дибромгидрин мезоэритрита BrH 2 C.СН(ОН).СН(ОН).CH 2 Br,
плавящийся при 135°; а второй — Br 2C.CH=CH.CH2 Br
— кристаллический, плавящийся при 53—54°, кипящий при 92—93° (15 мм), являющийся
главным продуктом превращения, образует при окислении KMnO 4
дибромгидрин рацемичного Э.
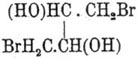 , плавящийся
при 83°; от последнего к Э. переходит через двуокись бутадиена: , плавящийся
при 83°; от последнего к Э. переходит через двуокись бутадиена:
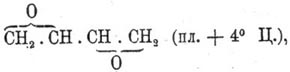 (плавится при
+ 4° Ц.), действуя на нее при 100° Ц. водой: С 4H6 О 2
+ 2Н 2 О = С 4 Н 6(OH)4
(Гринер). Тот же Э. может быть получен простым сливанием эквимолекулярных
растворов d.- и l.-Э. (Бертран и Макэн). Рацемический Э. плавится при 72° Ц.; он
необыкновенно легко растворим в воде; на воздухе расплывается; кристаллизуется в
тех же формах, что и d.- и l.-Э. (Вырубов); обладает сильно выраженным сладким
вкусом; оптически недеятелен; в спирте растворяется легче мезоэритрита. Описан
ряд его производных (Гринер, Бертран и Макэн). (плавится при
+ 4° Ц.), действуя на нее при 100° Ц. водой: С 4H6 О 2
+ 2Н 2 О = С 4 Н 6(OH)4
(Гринер). Тот же Э. может быть получен простым сливанием эквимолекулярных
растворов d.- и l.-Э. (Бертран и Макэн). Рацемический Э. плавится при 72° Ц.; он
необыкновенно легко растворим в воде; на воздухе расплывается; кристаллизуется в
тех же формах, что и d.- и l.-Э. (Вырубов); обладает сильно выраженным сладким
вкусом; оптически недеятелен; в спирте растворяется легче мезоэритрита. Описан
ряд его производных (Гринер, Бертран и Макэн).
Мезоэритрит, давно известный Э. (он же эритроглуцин, фицит, антиэритрит)
находится в свободном состоянии в водорослях Protococcus Vulgaris (Лами) и
Trentepohlia Jolithus (M. Бамбергер и А. Ландзидль), откуда и может быть
извлечен эфиром, а в виде орселиново-эритритового эфира, так называемого
эритрина, во многих лишаях и водорослях, каковы, например, Rocella Tinctoria,
Rocella fuciformis и особенно Rocella Montagn ë i,
откуда он может быть добыт омылением с помощью едкой щелочи или известкового
молока (Стенгоуз, Штреккер, Шунк, Лами, Вагнер, Гессе, Гофманн, Де Люинь):
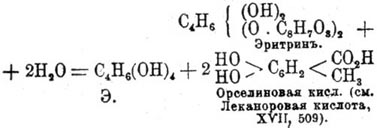
Кристаллизуется из концентрированных горячих водных растворов при прибавлении
(20 % по объему) спирта очень легко в призмах квадратной системы; плавится при
126° Ц. (Либерманн) и перегоняется без разложения при 330° (Либерманн); легко
растворим в воде, труднее в спирте и совсем нерастворим в эфире; сладок,
оптически недеятелен. При окислении азотной кислотой дает первоначально эритрозу
— (НО)Н 2 С.СН(ОН).СН(ОН).СОН,
а окончательно мезовинную кислоту (см. Винная кислота, l. с., Пржибытек). При
нагревании с концентрированным HI мезоэритрит превращается во вторичный йодистый
бутил Н 3 С.CHI.СН 2.CH3
(Де Люинь); описаны
многочисленные производные мезоэритрита, из которых можно отметить дихлоргидрин
СlН 2 С.СН(ОН).СН(ОН).СН 2 Cl,
образующийся при нагревании Э. с крепкой водной HCl, плавящийся при 125°
(Пржибытек), и ангидрид —
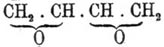 , получающийся
из предыдущего при действии KOH и представляющий жидкость, кипящую при 138°,
обладающую довольно сильным запахом и всеми реакциями органических окисей (см.
Окиси); легко полимеризуется (Пржибытек). При нагревании с муравьиной кислотой
мезоэритрит образует, между прочим, дивинил (см. выше; Генингер), а с P 2S5
— тиофен (см. Пааль и Тафель). , получающийся
из предыдущего при действии KOH и представляющий жидкость, кипящую при 138°,
обладающую довольно сильным запахом и всеми реакциями органических окисей (см.
Окиси); легко полимеризуется (Пржибытек). При нагревании с муравьиной кислотой
мезоэритрит образует, между прочим, дивинил (см. выше; Генингер), а с P 2S5
— тиофен (см. Пааль и Тафель).
А. И. Горбов. Δ.
|