Цитраконовая кислота
С5Н6О4 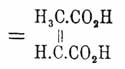 — двухосновная непредельная кислота ряда Сn Н 2n
— 4 О 4,
изомер кислот итаконовой и мезаконовой, получена впервые (Лассень) при сухой
перегонке лимонной кислоты; особенно обратила на себя внимание химиков после
работ Кекуле над нею и ее изомерами и над первыми членами этого ряда, кислотами
малеиновой и фумаровой (см.).
Не перечисляя многочисленных случаев образования этих кислот и их гомологов,
остановимся только на их взаимных отношениях, как они выяснены работами Фиттига
и его учеников (см. его свод "Liebig's Ann.", 304 ,
117, 1898). Как показал Фиттиг, эти кислоты могут быть легко получены следующим
путем. Сначала конденсацией альдегидов с янтарной кислотой (реакцией Перкина
ст.) получают параконовые кислоты (см.):
— двухосновная непредельная кислота ряда Сn Н 2n
— 4 О 4,
изомер кислот итаконовой и мезаконовой, получена впервые (Лассень) при сухой
перегонке лимонной кислоты; особенно обратила на себя внимание химиков после
работ Кекуле над нею и ее изомерами и над первыми членами этого ряда, кислотами
малеиновой и фумаровой (см.).
Не перечисляя многочисленных случаев образования этих кислот и их гомологов,
остановимся только на их взаимных отношениях, как они выяснены работами Фиттига
и его учеников (см. его свод "Liebig's Ann.", 304 ,
117, 1898). Как показал Фиттиг, эти кислоты могут быть легко получены следующим
путем. Сначала конденсацией альдегидов с янтарной кислотой (реакцией Перкина
ст.) получают параконовые кислоты (см.):
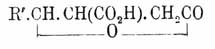
нагреванием с этилатом их изомеризуют и превращают в кислые эфиры итаконовых
кислот:
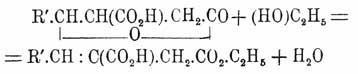
а из них омылением получают итаконовые кислоты; последние образуют при
перегонке ангидриды цитраконовых кислот; цитраконовые ангидриды, соединяясь с
водою (трудно), образуют Ц. кислоты, которые в хлороформном растворе на свету (в
присутствии следов брома) необыкновенно быстро превращаются (иногда почти
нацело) в мезаконовые кислоты.
[Первым продуктом R'.COH + CH 2(CO2H)CH2.CO2 H
является окси-кислота: R'.CH(OH).CH(CO 2 H)СН 2.СО 2 Н,
которая затем, теряя воду, образует лактонокислоту (параконовую)]
Несколько сложнее следующий путь: из однозамещенного дибромацетоуксусного
эфира, т. е. из СНВr 2.СО.СН.R'.СО 2 С 2H5
(R' = CH3 С 2H5
и т. д.) действием щелочи
получают соль соответственной мезаконовой кисл. (Демарсэ, Павлов, Горбов, Клоэз,
Вальден и, особенно, В. Семенов; ход превращения не выяснен окончательно и
непонятно, почему оно не удается для незамещенного ацетоуксусного эфира), а из
свободной кисл., при действии хлористого ацетила, — ангидрид цитраконовой кисл.
Полученные тем или другим путем изомеры, иногда образующиеся в смеси, легко
разделяются. Для цитраконовых кисл. является характерной способность даже в
водном растворе переходить при температуре кипения раствора в ангидрид, летучий
с парами воды, между тем как итаконовые и мезаконовые кислоты совершенно не
перегоняются в этих условиях. [В связи с этим находится наблюдение В. Семенова,
что ангидрид диметилцитраконовой кисл. — С 7 Н 8 О 3,
растворенный в воде, даже при продолжительном стоянии раствора не дает кислоты С 7 Н 10 О 4.]
Итаконовые кисл. легко отделяются от мезаконовых с помощью Ва- или Са-солей,
очень трудно растворимых для итаконовых кисл., особенно в горячей воде, и столь
легко растворимых для мезаконовых кисл., что их растворы начинают выделять соль
только сгущенные до сиропообразной. консистенции. Ита- и цитраконовые кислоты не
имеют, собственно говоря, определенной темп плавления, так как их плавление
совершается с образованием ангидридов и, след., зависит от быстроты нагревания
кислоты, причем обязательно должно иметь место перегревание; вообще же
цитракислоты становятся жидкими уже ниже 100° (исключение — фенилцитраконовая,
пл. между 105 и 108°; Фиттиг, Брук), а итакислоты — значительно выше.
Мезакислоты обыкновенно плавятся еще выше (изопропилмезаконовая плав. ниже своей
итакислоты) и отличаются, главным образом, резкой темп. пл., так как они при
этом почти не разлагаются и даже при несколько более высоких температурах
возгоняются без разложения; незначительная часть кисл. теряет, однако, воду,
изомеризуясь в Ц. ангидрид (при диметилмезаконовой С 7 Н 10 О 4
Краффт подметил и
одновременное образование ничтожных количеств диметилитаконового ангидрида).
Ита- и цитракислоты имеют свои ангидриды; при перегонке под обыкновенным
давлением ангидриды итакислот переходят (иногда почти нацело) в ангидриды
цитракислот, но превращение это не одностороннее (по Фиттигу), а обратимое; при
перегонке под уменьшенным давлением итаангидрид обыкновенно не изменяется,
итакислота же и в этих условиях (благодаря более высокой температуре опыта) дает
немного цитраангидрида. [Если это наблюдение верно и не объясняется, напр.,
недостаточным для окончания процесса временем наблюдения или же разностью
температур (см. о взаимных переходах белого и красного фосфоров), то отношения
эти по существу отличны от отношений малеиновой и фумаровой кислот и напоминают
скорее взаимные отношения различных кристаллографических разновидностей серы.]
Нагревание цитракислоты в водном растворе при 180—150° (в запаянных трубках)
превращает ее в итакислоту. При нагревании с НСl, НВr и в подходящих условиях с
H 2SO4
итакислоты обратно превращаются в параконовые кисл. Подобно тому, как малеиновая
и фумаровая кисл. при гидрогенизации дают одну и ту же янтарную кислоту, так
ита-, цитра- и мезакислоты образуют, соединяясь с водородом, тождественные
пировинные (метил-, этил- и т. д. янтарные) кисл.; легче всех гидрогенизуются
цитракислоты, за ними следуют мезакислоты; итакислоты гидрогенизуются очень
трудно. Под влиянием кипячения с едкими щелочами эти кислоты изомеризуются,
причем превращение не доходит до конца и
для состава конечной смеси
совершенно безразлично, из какого ряда — ита-, цитра- или меза- — исходит при
опыте. Легче и полнее других изомеризуются цитракислоты, превращаясь в главной
массе в итакислоты, труднее — мезакислоты; при достаточной крепости щелока
превращение их почти полное (наименее значительно оно для самой мезаконовой
кислоты C 5H6O4);
конечным продуктом изомеризации является обыкновенно итаконовая кислота со
сравнительно незначительными примесями изомерных кислот (относительные
содержания последних значительно колеблются для различных кислот. [В некоторых
случаях итакислота, в свою очередь, изомеризуется еще в атиконовую кислоту.] О
дальнейших подробностях см. Фиттиг. В заключение привожу характерные данные для
настоящих незамещенных: Ц., итаконовой и мезаконовой кислот. Ц. кислота
кристаллизуется из воды в одноклиномерных призмах (похожих на иглы — из смеси
эфира и лигроина); темп. пл. 80° (старые данные) — 91° (Фиттиг и Лангворти);
легко растворима в эфире, трудно — в холодном хлороформе, очень мало — в CS 2,
C6H6 и
лигроине. Нагретая с водою до 120° дает итаконовую, а до 180° — мезаконовую
кислоту; при кипячении с NaOH переходит в итаконовую, а затем большею частью в
мезаконовую; под влиянием P é nicillium
образует кислоту C 5H8O5
(Ле-Бель, см. Стереоизомерия); ангидрид кипит под давлением 15 мм при 99
— 100°. Итаконовая кисл. Н 2 С:С(СО 2 Н).СH 2 СО 2 Н
плавится с разложением при 161°; о реакциях ее см. выше; ангидрид плав. при 68°,
кипит под давл. 30 мм при 139 — 140°; под обыкн. давл. переходит в Ц. ангидрид.
Мезаконовая кислота —
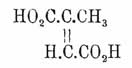 — получается
из метилдибромацетоуксусного эфира или изомеризацией предыдущих кислот; удобна
изомеризация эфирно-хлороформного раствора Ц. кислоты под влиянием брома и
солнечного света; плав. при 202 — 203°; реакции ее см. выше. Очень часто в
современных учебниках органической химии она называется транскислотою, но,
насколько можно судить, отношения ее другие, чем типичной транскислоты —
фумаровой; с современной физико-химической точки зрения эти отношения должны еще
считаться недостаточно выясненными, а потому и название преждевременным. — получается
из метилдибромацетоуксусного эфира или изомеризацией предыдущих кислот; удобна
изомеризация эфирно-хлороформного раствора Ц. кислоты под влиянием брома и
солнечного света; плав. при 202 — 203°; реакции ее см. выше. Очень часто в
современных учебниках органической химии она называется транскислотою, но,
насколько можно судить, отношения ее другие, чем типичной транскислоты —
фумаровой; с современной физико-химической точки зрения эти отношения должны еще
считаться недостаточно выясненными, а потому и название преждевременным.
А. И. Горбов. Δ .
|