Большая Советская
Энциклопедия
|
|
|
|
источник статьи: Большая Советская Энциклопедия |
|
Сигма- и пи-связи (s- и p-связи), ковалентные химические связи, характеризующиеся определенней, но различной пространственной симметрией распределения электронной плотности. Как известно, ковалентная связь образуется в результате обобществления электронов взаимодействующих атомов. Результирующее электронное облако s-связи симметрично относительно линии связи, т. е. линии, соединяющей ядра взаимодействующих атомов. Простые связи в химических соединениях обычно являются (т-связями (см. Простая связь). Электронное облако p-связи симметрично относительно плоскости, проходящей через линию связи (рис. 1, б), причём в этой плоскости (называемой узловой) электронная плотность равна нулю. Употребление греческих букв Если между атомами в молекуле возникают одновременно как s-, так и p-связи, то результирующая связь является кратной (см. Кратные связи, Двойная связь, Тройная связь, а также Валентность).
Лит.: Пиментел Г., Спратли Р., Как квантовая механика объясняет химическую связь, пер. с англ., М., 1973; Шусторович Е. М., Химическая связь, М., 1973. Е. М. Шусторович. 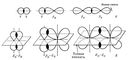 Рис. 1. Схематическое изображение пространственной ориентации орбиталей при образовании s-связи в результате s — s-, s — ps-, ps — ps-взаимодействий (а) и p-связи в результате pp — , pp — , dp — dp — взаимодействий (б). 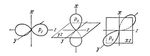 Рис. 2. Схематическое изображение облаков px-, ру-, pz- электронов. Показаны оси декартовых координат и узловые плоскости px - и ру-орбиталей. |