Тиглиновая кислота
(хим.) — С 5 Н 8 О 2
= СН 3 —СН=С(СН 3)—СО 2 Н
[метил(3)бутен(2) кислота(4)], метилкротоновая (твердая) кислота, изомер
пентеновых кислот (см.), в виде глицерида заключается в кротоновом масле [Кроме
Т. кисл. там имеются еще летучие и нелетучие кислоты (миристиновая,
лауриновая).], где и открыта (Гейтером и Фрёлихом) и откуда она получила свое
название (Croton tiglium). В виде изобутилового эфира она входит в состав той
сложной смеси эфиров, которая находится в римской ромашке (Кёбиг, Копп,
Пагенштехер, Бейльштейн и Виганд). Т. кисл. может быть получена при действии
треххлористого фосфора на эт-метокзаловый эфир (Франкланд и Дюппа):
СН 3 —СН 2 —(НО)С(СН 3)—СО 2 С 2H5
= СН 3 —СН=С(СН 3)—СО 2H
+ C2H6O;
она образуется при сухой перегонке α-метил-β-оксимасляной кислоты (Рорбек):
СН 3 —СН(ОН)—НС(СН 3)—CO2 H
= СН 3 —СН=С(СН 3)—СО 2 H
+ Н 2 О
или при нагревании ее с перегнанным йодистым водородом (Рюккер); при
окислении кислородом воздуха тиглинового альдегида [Получен Фёлькелем при сухой
перегонке гваяковой смолы.] (Герциг); при нагревании до 120—130°С (30 час.)
эквимолекулярных количеств обыкновенного альдегида, пропионового натрия и
пропионового ангидрида, т. е. реакцией Перкина (Китрейбер):
СН 3 —СНО + СН 2 (СН 3)—СО 2 H
= СН 3 —СН=С(СН 3)—СО 2 H
+ Н 2 О;
при долговременном кипячении ангеликовой кислоты (Демарсэ; реакция открыта
Гемилианом, нашедшим превращение в этих условиях жидкой кротоновой в твердую
кротоновую кислоту), нагревании ее (до 120°) с водою (1 г кисл. + 15 куб. стм H 2 O),
10% едким натром (при 100°, Фиттиг) или крепкой серной кисл. (Демарсэ); при
нагревании с серной кисл. α-этилакриловой CH 2=C(C2H5)—CO2 H
(Кондаков, В. Семенов); при действии брома в отсутствие света на ангеликовую
кислоту (Фиттиг) и при отнятии амальгамой натрия брома от продукта
взаимодействия ангеликовой кислоты с бромом (дибромтиглиновой кисл., см. ниже,
Е. Шмидт). Для добывания более удобно омыление масла римской ромашки водным или
лучше (Демарсэ) спиртовым едким кали; по окончании реакции спирты отгоняют,
остающиеся калиевые соли разлагают серною кислотою, извлекают кислоты эфиром, из
вытяжки отгоняют эфир и остаток фракционируют. Из порций, кипящих около 185°,
выкристаллизовывается уже при обыкновенной температуре ангеликовая кислота,
которая выпадает и при охлаждении (сначала льдом, а потом и охладительной смесью
снега с солью) фракций, кипящих 185—190°; из порций, кипящих выше 190°, при
охлаждении выпадает Т. кислота; последовательным отделением кристаллов,
выпадающих при охлаждении, и фракционировкой полного разделения кислот нельзя
достигнуть, и дальнейшее очищение их основано на свойствах кальциевых солей:
кальциевая соль ангеликовой кисл. растворимее в холодной воде, а Т. в горячей;
последняя растворяется в спирту, а первая почти не растворима (Фиттиг). Вопрос о
том не является ли в этом случае Т. кисл. продуктом изомеризации заключающейся в
масле ангеликовой кисл. не решен пока окончательно. Чистая Т. кисл.
кристаллизуется в трехклиномерных таблицах и призмах; обладает запахом,
напоминающим запах бензойной кислоты; плавится при 64,5°; кип. при 198,5°
(Копп); легко растворима в горячей воде и трудно в холодной; не восстановляется
амальгамой натрия, но йодистым водородом (в присутствии фосфора) превращается в
(рацемическую) метилэтилуксусную кисл. СН 3 —СH 2 —СH(СН 3)—СО 2 Н,
предварительно образуя как продукт прямого соединения йодометилэтилуксусную
кисл.:
СН 3 —СН=С(СН 3)—CO2 H
+ HJ = СН 3 —СН 2 —СJ(СН 3)—СО 2 Н.
При сплавлении с едким кали дает соли уксусной и пропионовой кисл.:
СН 3 —НС=С(СН 3)—CO2H
+ H2 O + O = СН 3 —СО 2 Н
+ СН 3 —СH 2 —СО 2 Н
(реакция до известной степени обратна реакции образования Т. кисл. из
уксусного альдегида и пропионовокислого натрия, см. выше). С бромом дает
дибромтиглиновую кисл. C 5H2Br2O2
(тождественную c кислотою, получающеюся из ангеликовой при действии
эквивалентного количества брома и медленном ведении реакции присоединения). При
окислении хамелеоном получены уксусный альдегид, углекислота, уксусная и
тиглицериновая (С 5H10 О 4
= С 5H8 О 2
+ Н 2 О + О)
кислоты (Кондаков, Бейльштейн и Виганд, Фиттиг и Пеншук). Строение Т. кислоты
было предметом многочисленных исследований, но до сих пор не может считаться
окончательно установленным. До возникновения стереохимических воззрений (см.
Стереоизомерия и Стереохимия) большинством исследователей принималось, что
отношение между ангеликовой и Т. кислотами отвечает отношению между жидкой и
твердой кротоновыми (см.) кислотами, а так как жидкой кротоновой кислоте
приписывалась структурная формула — СН 2 =СH—СН 2 —СО 2 Н,
а для твердой — СН 3 —СН=СН—СО 2 Н,
то и ангеликовой к. придавалась формула — СН 2 =СН—СН(СН 3)—СО 2 Н,
а Т. — приведенная выше. Но эти формулы не объясняли след. фактов. Шмидтом было
найдено, что ангеликовая и Т. кислоты при действии йодистого водорода образуют
две йодовалерьяновых кисл. C 5H8O2 + HJ =
C6H9JO2,
различных по темп. плавления и другим физическим свойствам, но тождественных,
как нашел Фиттиг, по отношению к раствору соды, при действии которого обе
кислоты распадаются на йодистый натрий, углекислый газ и псевдобутилен: C 5H8JO2Na
= C4H8 + NaJ + CO2;
подобная реакция, как установил Эрленмейер (старший), должна считаться
характерной для β-галоидокислот, а между тем ясно, что при указанных формулах
можно ожидать из обеих кислот только одной (рацемической)
β-йодо-α-метилнормальной масляной кислоты (формула дана выше). К этому
присоединилось (ошибочное, как мы теперь знаем на основании работ В.
Вислиценуса) наблюдение, по которому продукты присоединения брома к ангеликовой
и Т. кислотам были признаны тождественными [При действии брома на ангеликовую
кислоту действительно получается дибромтиглиновая кислота (Цагенштехер, Фитгиг),
но если действовать обратно ангеликовой кислотою на избыток охлажденного брома,
то образуется наряду с небольшим количеством дибромтиглиновой кислоты и отличная
от нее дибромангеликовая (Пюкерт, В Вислиценус).], и Фиттиг, обсуждая
приведенные факты, пришел к заключению, что структурные формулы не в состоянии
передать изомерии этих кислот. В. Вислиценус в своей известной статье "Die r äumliche
Anordnung der Atome in organischen Molekü len"
(см. Стереоизомерия) высказал предположение, что изомерия кислот —
пространственная, и, приравнивая ангеликовую кислоту малеиновой, а Т. —
фумаровой, дал им стереохимические формулы, проекции которых на бумаге след.:

Это воззрение встретило сильного противника в лице А. Михаэля, указавшего,
что многие из толкований реакций образования этих кислот, данные Вислиценусом на
основании таких формул, совершенно не отвечают действительно наблюдаемым
процессам, и тем не менее, за неимением лучшего, воззрение Вислиценуса должно
признать пока пользующимся наибольшим правом гражданства
[Насколько шатки эти формулы, видно
из следующего. Байер, обсуждая стереохимические формулы симметрично
двузамещенных янтарных кислот — НО 2 С—СНХ—СНY—СО 2 Н
(см. Стереоизомерия), высказал убеждение, что в органических соединениях
наиболее энергичное стремление к соединению, наиболее энергичное влияние друг на
друга должно быть приписано не электроположительным с электроотрицательными
группами, а электроположительными между собою, и как на доказательство этого
указал на меньшую стойкость уксусной кислоты (+)CH 3—CO2 H(—)
сравнительно с этаном (+)CH 3—CH3 (+).
Если подобную аргументацию приложить к приведенным выше формулам ангеликовой и
Т. кислот, то мы должны были бы приписать
им обратные формулы, т. е. признать
Т. кислоту, как более прочную, за —
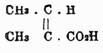 , а ангеликовую
за — , а ангеликовую
за — 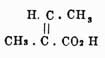 , но
очевидно, что благодаря такому перемещению формулы не стали бы более твердо
доказанными.]. Нельзя, однако, не обратить внимания на то, что между Т. кислотою
и кислотами ангеликовой и α-этилакриловой существуют, по-видимому, те же
отношения, которые наблюдаются для двуосновных кислот: мезаконовой,
цитраконовой, итаконовой и атиконовой, с тою, впрочем, разницей, что этих
одноосновных кислот пока известно три, а не четыре изомера, и нельзя пока
сказать, может ли ангеликовая или α-этилакриловая отвечать атиконовой. , но
очевидно, что благодаря такому перемещению формулы не стали бы более твердо
доказанными.]. Нельзя, однако, не обратить внимания на то, что между Т. кислотою
и кислотами ангеликовой и α-этилакриловой существуют, по-видимому, те же
отношения, которые наблюдаются для двуосновных кислот: мезаконовой,
цитраконовой, итаконовой и атиконовой, с тою, впрочем, разницей, что этих
одноосновных кислот пока известно три, а не четыре изомера, и нельзя пока
сказать, может ли ангеликовая или α-этилакриловая отвечать атиконовой.
А. И. Горбов. Δ .
|