Пиримидины
или метадиазины, подобно пиразинам (см.) и пиридазинам
(см.), имеют замкнутую группировку, из 4 атомов углерода и 2 ат. азота, но
находящихся друг к другу в мета-положении. По своему химическому характеру П.
представляют слабые основания и могут быть рассматриваемы как циклические
амидины. Для определения мест боковых цепей атомы углерода в П. обозначаются
греческими буквами в след. порядке
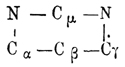 . Этот класс
соединений сравнительно мало разработан, и только некоторые из его
представителей имеют интерес или как продукты конденсации жирных нитрилов, или
же как вещества, принадлежащие к группе мочевой кислоты. Получаются П.
конденсацией β-дикетонов
с амидинами: . Этот класс
соединений сравнительно мало разработан, и только некоторые из его
представителей имеют интерес или как продукты конденсации жирных нитрилов, или
же как вещества, принадлежащие к группе мочевой кислоты. Получаются П.
конденсацией β-дикетонов
с амидинами:
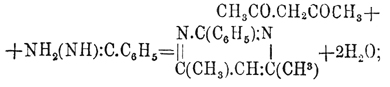
Этой реакцией возможно получать и некоторые производные П.; так, из амидина и
бромистого триметилена получаются тетрагидро-П.:
NH2(NH) = C—C6H5
+ Br—СН 2 —СН 2 —СН 2 Вr
= С 6 Н 5 С
= (N—NH) = (СН 2)2
= СН 2
+ 2НВr;
с эфирами кетокислот образуются окси-П., с эфирами
β-кетодикарбоновых кислот —
эфиры оксипиримидинкарбоновых кислот. При этих реакциях интересно то, что группа
NH не реагирует с СО 2 Н,
как обыкновенно, т. е. давая (—CO—N=), а в реакцию вступает NH и (—СН 2 —СО 2 H)
и образуется группировка (—CH=C(OH)—N=). Второй способ получения П., вполне не
разъясненный, состоит в конденсации жирных нитрилов в присутствии металлического
натрия при 150°. При этом три молекулы нитрила образуют α-амидо-П., или
таналкин, который азотисто-натриевой солью легко переводится в α-окси-П.:
3CH 3—CN = μ, γ (CH3)2C4HN2(NH) α.
Вероятно, здесь сначала образуется динитрил типа R—C(NH)—CHR—CN; возможно, что в
реакции участвует и более 3 мол. нитрила, так как всегда при этом получается
NaCN. Как на пример П. можно указать на кианкониин, или
α, μ-диэтил-β-метилпиримидин
С 4 НN 2 (С 2 Н 5)2 (СН 3),
масло, кипящее при 205°, по запаху и по своему физиологическому действию
напоминающее алкалоид кониин. Кетопроизводные гидропиримидинов известны под
названием урацилпроизводных и находятся в тесной связи с мочевой кислотой (см.).
Бензопроизводные П. — см. Хиназолины.
Д. А. Хардин. Δ .
|