Нитрозожелезисто-синеродистые соединения
(хим.) или нитрозо-, а также нитропруссиды — замечены впервые
Л. Гмелином. Если растворить желтую соль (см.) в разведенной азотной кислоте
[Берут (Wild) 8 весов. частей желтой соли в порошке, обливают 12 ч. воды и
прибавляют 15 ч. азотной кислоты уд. в.
1,24] и подвергнуть этот раствор
слабому нагреванию, то выделяется циан, синильная кислота, углекислый газ, азот;
раствор содержит азотно-кислые калий и железо и нитропруссидный калий
K2FeC5N5(N O);
так как эта соль дурно кристаллизуется, то прибавляют избыток соды и извлекают
спиртом, который растворяет только натриевую соль, хорошо кристаллизующуюся в
больших рубиново-красных кристаллах ромбической системы и обладающую составом Na 2FeC5N5(NO)
+ 2 Н 2 O
(Жерар). Из этой соли двойным разложением можно получить другие соли, а из Ag 2FeC5N5 (NO),
действием соляной кислоты, или из BaFeC 5N5.NO,
действием серной, и нитропруссидную кислоту H2FeC5N5.NO,
которая выделяется из водного раствора при испарении на холоде в темно-красных
расплывчатых кристаллах. Эта кислота, получается также (Гадов, Штэделер) при
действии азотистой кислоты на железисто-синеродисто-водородную в следующие две
фазы:
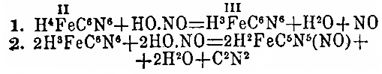
При действии амальгамы натрия на раствор
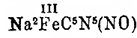 получен (К. А.
Гофман, 1895) амидопруссидный натрий получен (К. А.
Гофман, 1895) амидопруссидный натрий
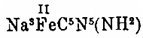 , который
кристаллизуется с 2 1/2H2 O
в виде янтарно-желтых призм; окислителями и при действии NO и HNO 2
эта соль превращается обратно в Na 2C5N5 (NO).
Нитропруссидный натрий есть реактив на сернистые калий, натрий и пр. (но не на
сероводород — нужно прибавить NaOH или NH 3),
и притом очень чувствительный — растворы окрашиваются в красивый пурпурово-синий
цвет; окрашивание очень непостоянно. , который
кристаллизуется с 2 1/2H2 O
в виде янтарно-желтых призм; окислителями и при действии NO и HNO 2
эта соль превращается обратно в Na 2C5N5 (NO).
Нитропруссидный натрий есть реактив на сернистые калий, натрий и пр. (но не на
сероводород — нужно прибавить NaOH или NH 3),
и притом очень чувствительный — растворы окрашиваются в красивый пурпурово-синий
цвет; окрашивание очень непостоянно.
С. Колотов. Δ.
|