Марганец, химический элемент
(Manganè se — франц. и англ.;
Mangan — нем.; Mn = 55,09 [Среднее из 55,16 (Dewar и Scott, 1883) и 55,02
(Marimac, 1884)]. Уже древние знали о существовании главной руды М., пиролюзита,
употребляли этот минерал при приготовлении стекла (Плиний Ст.) и уподобляли его
магнитному железняку, хотя и знали, что он железа не притягивает. Шееле, в своей
статье "De magnesia nigra" (1774), положил начало изучению M., а вместе с тем и
хлора, кислорода и бария (в им исследованном материале присутствовала и ВаО). В
том же году был получен и металлический М. Ганом. Кроме magnesia nigra
существовало (XVI в.) название того же минерала — lapis manganensis;
отсюда и ведет свое начало
современное наименование металла. Соединения М. очень распространены в природе,
но обыкновенно в малых количествах. Богатые металлом руды и минералы сдедующие:
пиролюзит MnО 2,
браунит Mn2O3,
гаусманнит Mn3O4,
псиломелан (Mn, Ва)О.MnО 2,
манганит Mn2O2(OH)2,
марганцевый шпат MnСО 3
обыкновенно в изоморфных смешениях (Mn,Fe)CO 3, (Mn,Ca,Mg)CO3,
родонит MnSiO3.
В малых количествах М. находится в большинстве силикатов, а потому присутствует
в почвах, находится в золе растений и в костях животных. Встречается в виде
сернистых соединений MnS и MnS 2,
a также образует изоморфные смешения с другими сернистыми металлами. В
самородном виде не встречается, потому что очень легко окисляется и труднее
железа восстанавливается. Существует несколько путей для получения
металлического М.: через восстановление углем окислов при сильном калении (John,
Deville, Moissan), при сплавлении MnCl 2
с CaF 2 и
металлич. Na (Brunner), путем электролиза крепкого раствора MnCl 2
(Bunsen). M. обыкновенно не
получается чистым, содержит углерод, кремний. В чистом виде получают из
амальгамы; амальгаму же можно получить, действуя амальгамой натрия на раствор
MnCl 2, или
электролизом того же раствора, употребляя катод из ртути; по полной отгонке
ртути, что совершается при 440° (Moissan), остается порошкообразный металл.
Водород и окись углерода более или менее легко действуют на многочисленные
окислы М., за исключением закиси MnО; ее они не восстанавливают даже при 600°
(Wright и Luff), а потому все они водородом превращаются в MnО; последняя при
сплавлении с металлическим алюминием, под известью и плавиковым шпатом, дает
довольно чистый металл (до 97% — Greene и Wahl, 1893); при действии магния на
сплав MnCl 2 + КСl 2
(1 в. ч. + 2 в. ч.) получается королек очень чистого металла (Glatzel, 1889),
удел. вес которого, d
20°/20° = 7,3921. По цвету М.
приближается к железу, но обладает красноватым отливом, подобно висмуту; ломок и
очень тверд — режет сталь, стекло; совершенно не притягивается магнитом, если не
содержит железа; теплоемкость 0,1217 (с содерж. Si, при 14° — 97°, Regnault);
плавится труднее железа, при 1900°; по-видимому, летуч при температурах немного
высших точки плавления [Как показали опыты нагревания до белого каления в
фарфоровой трубке в струе окиси углерода, водорода или азота (Lorenz и Heusler,
1892). Ни с H, ни с CO не получается при этом летучего соединения, подобного NiC 4O4,
как показало спектроскопическое исследование пламени H или СО, зажженных при
выходе из трубки]. М. легко выделяет водород с разведенными кислотами, при чем
получаются соли закиси MnХ 2;
даже на подогретую воду он действует и окисляется при обыкновенной температуры
на воздухе. Порошкообразный М., из амальгамы, еще легче окисляется на воздухе и
под водой; при взбалтывании его с водой и воздухом получается перекись водорода.
Сплавы марганца с железом указаны ниже в ст. М. (металлургия), марганцевая
сталь, ферроманган, белый чугун. Сплавы с медью очень похожи на сплавы олова с
медью (см. Манганин). Сплав М. (80%) с цинком (5%) и медью (15%), так назыв.
марганцевый нейзильбер, получается при восстановлении углем окислов, белого
цвета, легко обрабатывается и хорошо полируется. О марганцовой бронзе см.
Бронза. Из жидкой амальгамы отжиманием получена кристаллическая MnHg 5
[О. Prelingep (1893). Жидкая амальгама была получена, по Муассану, электролизом,
по отгонке всей ртути в струе водорода при темно-красном калении остался серый
пористый М., уд. в. 7,4212, такой М. реагирует с азотной кислотой с
воспламенением, из нашатырного раствора выделяет аммиак и водород, а также
следующие металлы из их соляных растворов — Sn, Рb, Sb, As, Bi, Сr, Fe, Со, Ni,
Сu, Zu и Cd]. Спектр М. дают искры от вторичной спирали, полученные на
поверхности раствора MnCl 2,
или свет дуги между электродами из металлического М. Спектр содержит много
линий: в оранжевой части (3 л.), в синей (5 л.), в фиолетовой (2 л.). Спектр от
MnO — полосчатый; источником служит огонь при бессемеровском процессе.
Кислородные соединение М. так многочисленны и разнообразны по свойствам,
как ни для одного другого элемента; известны следующие — MnО, Mn 3O4,
Mn2O3, MnО 2,
MnО 3, Mn2O7.
Состав высшего окисла определяет положение М. в 7-й группе периодической
системы. Низший окисел есть основание; соли, отвечающие MnО, закиси, получаются
при действии кислот и на металлический М., и на все его окислы, при чем из
высших выделяется лишний кислород
Mnn О m
+ 2nHX = nМnХ 2 +
nН 2O + (m — n)O;
при употреблении соляной кислоты выделяется хлор:
Mnn О m
+ 2mHCl = nMnCl2 + mH2O + (m — n)C12.
При обыкн. темп. могут существовать все окислы, при нагревании постоянен один
— Mn 3O4;
при нагревании на паяльной лампе в тигле при доступе воздуха МnО поглощает
кислород, а МnО 2
теряет его, также и Мn 2 О 3
— в обоих случаях образуется
Мn 3 О 4,
а потому при количественном анализе применяется взвешивание в виде этого окисла;
высшие окислы МnО 3
и Мn 2 О 7
в свободном виде очень непостоянны, даже при обыкн. темп. Основные свойства МnО
очень значительны; по мере накопления кислорода основные свойства слабеют, но
они могут быть подмечены даже для Мn 2 О 7;
с другой стороны, МnО 2,
будучи основанием крайне слабым, проявляет уже свойства слабого кислотного
окисла; ангидридные свойства МnО 3
и особенно Мn 2 О 7
вполне резко выражены.
Закись М. удобнее всего получается при нагревании в струе водорода высших
окислов или углекислого М. в виде зеленоватого порошка; она превращается в
прозрачные, зеленые, блестящие октаэдры, если водород, в котором ее нагревают,
содержит некоторое количество хлористого водорода; эти кристаллы, не изменяя
формы, превращаются в Мn 3 О 4
при нагревании на воздухе. Гидрат закиси Мn(ОН) 2
осаждается щелочами из растворов солей закиси в виде белого осадка, быстро
буреющего на воздухе вследствие окисления. По химическим свойствам МnО очень
походит на MgO; основные свойства МnО резче; соли МnХ 2
сходны то с солями MgX 2,
то с солями FeX 2, NiX2, CuX2.
Хлористый М. (безводный)
MnCl 2 получается
при прямом соединении М. и хлора, при нагревании в токе хлористого водорода МnО
или МnСО 3;
представляет светло-розовые кристаллические листочки, при красном калении
плавится и при действии влажного воздуха дает НСl и высшие окислы М. В растворе
MnCl 2 получают
обыкновенно из остатков от добычи хлора; здесь всегда находится FeCl 3,
которое с МnСО 3
дает MnCl 2, a Fe(OH)3
осаждается; иной раз в исходном растворе присутствуют еще соли меди, бария или
кальция, тогда сероводородом удаляют медь, а сернистым аммонием осаждают весь М.
в виде тельно-розового осадка MnS, растворимого легко в соляной кислоте. Если
кристаллизация из крепкого раствора MnCl 2
совершается при
15-20°, то осаждаются кристаллы одноклин. сист. состава MnCl 2.4H2 O;
чтобы обезводить эту соль нужно нагревать в токе HCl-газа. МnВr 2.4H2 O
вполне похож на предыдущую соль; MnJ 2.4H2 O
в отсутствии воздуха может быть обезвожен и даже расплавлен, в присутствии
воздуха нагревание приводит к выделению паров йода, причем получаются окислы М.
Сернокислый MnSO4
получается при сильном нагревании тестообразной смеси пиролюзита и крепкой
серной кислоты, при чем происходит выделение кислорода. По охлаждении —
извлечение водой и кристаллизация; из крепкого раствора ниже 6° выделяются
кристаллы MnSO 4.7H2 O,
изоморфные с железным купоросом, при 7° -20° — кристаллы MnSO 4.5H2 O,
изоморфные с медным купоросом; известны также гидраты и другого состава. Ниже
200° все эти гидраты дают MnSO 4.H2 O
(Грэм) — желтовато-розоватый порошок; этот гидрат теряет воду выше 200°, при чем
теряет и окраску, разлагается только при красном калении, превращаясь в Mn 3O4.
Двойные соли, как при других купоросах, имеют состав M 2Mn(SO4)2.6H2O.
Азотнокислый М., Мn(NO 3)2.6H2O,
при нагревании плавится, кипит при 129,5°, разлагаясь и выделяя черную окись Mn 2O3.
Углекислый
М., 5MnCO3.Mn(OH)2
(H. Rose), получается в виде
белого осадка при действии соды на растворы МnХ 2;
он очень трудно растворим в воде (1 ч. в 8000), а потому применяется при
количественном анализе для отделения; уже при обыкн. темп. осадок окисляется, а
при накаливании дает красную Mn 3O4.
При действии на раствор солей MnХ 2
цианистым калием получается желтоватый осадок синеродистого М., MnСу 2,
который очень непостоянен. Подобно желтой соли (см.), и здесь имеется двойная
соль К 4 МnСу 6.3H2 O,
кристаллизующаяся в виде темно-сине-фиолетовых квадратных пластинок; они легко
теряют воду и дают раствор, к удивлению, почти не окрашенный или слабо-желтый.
При стоянии на воздухе такого раствора совершается окисление
2K4MnCy6 + H2 O
+ О = 2К 3 MnСу 6
+ 2КОН;
получается новая соль, аналогично превращению желтой соли в соль Гмелина
(см.) но там для этой реакции требуется энергический окислитель, здесь же она
совершается очень легко, при действии кислорода воздуха. Эта двойная соль
К 3 МnСу 6,
относящаяся к окисному типу — МnХ 3,
кристаллизуется в виде темно-красных призм; при действии амальгамы калия с водой
она восстанавливается в предыдущую.
Двуокись М. МnО 2
[Ниже будут рассмотрены соединения
окисного типа: но сначала должно сказать о МnО 2,
неправильно именуемой "перекисью" Этот окисел не есть перекись свинца, это суть
двуокиси, металл в
них четырехэквивалентен; их структурные формулы такие
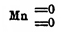 и и
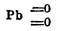 ,
с кислотами они не дают перекиси
водорода, хотя последняя в присутствии аммиака и осаждает из раствора МnХ 2
двуокись; состав осадка Mn 6O11=5MnO2 MnO
(A. Carnot)], подобно РbО 2,
обладает слабыми кислотными свойствами, а потому образует с основаниями
солеподобные соединения, манганиты. Важнейшая руда. М., пиролюзит, есть почти
чистая двуокись, встречается в виде квадратных кристаллов и в виде масс,
кристаллического характера; обладает стально-серым или черным цветом и
металлическим блеском, уд. в. 4,82. Из солеподобных соединений в природе
находятся псиломелан — (Мn, Ва)О.2МnО 2,
манганит Мn 2O2 (ОН) 2,
который можно представить чрез МnО. МnО 2.H2 O
[В природе встречается обыкновенно
вместе с известковым и тяжелым
шпатом]. Искусственно МnО 2
можно получить, если промыть азотной кислотой, при кипячении, остаток после
слабого каления Mn(NO 3)2
или MnСО 3 при
доступе воздуха; в первом случае промывается черная окись Mn 2O3,
во втором — красная закись-окись Mn 3O4
(см. ниже); так как в обоих случаях остается до промывании двуокись, то и Mn 2O3,
и Mn 3O4
должно считать солеподоб.
веществами, как Pb 2O3
и Pb 3O4
(сурик), которые точно так же при действии HNO 3
дают PbO 2.
Двуокись М. можно получить и в виде гидрата, если действовать на раствор MnХ 2
раствором хлора или брома в едкой щелочи или если промыть гидрат Mn 2O3
азотной кислотой; такой гидрат MnО 2,
промытый водой, растворим с бурым цветом (Gorgen); раствор обладает кислой
реакцией, сохраняется в течение недель; малые количества щелочей или кислот
осаждают гидрат (свертывают) [Получены след. калиевые соли этой кислоты: K 2O.5MnO2
— желтый осадок, образующийся
при действии углекислоты на раствор K 2MnO4; K2O.MnO2
— темно-бурый порошок,
получается при нагревании KMnО 4,
второй манганит водой разлагается на КОН и первый манганит]. Но двуокись М.
обладает и свойствами основными; если действовать при охлаждении на MnO 2,
разболтанную в эфире, хлористым водородом, то получается зеленый раствор, по
всей вероятности MnCl 4
(аналогично действуют и НВк и HJ); при -26° MnCl 4
почти не разлагается в водном растворе (Vernon, 1892); с крепкой плавиковой
кислотой получается из MnО 2
несомненно MnF 4,
потому что бурый раствор, получающийся при этом с KF, дает розовый осадок
состава K 2MnF6.
Если смешать 1 часть марганцево-кислого калия (см. ниже) с 5 ч. Н 2 SО 4
и 1 1/2
ч. H 2 O, то по
мере выделения кислорода раствор делается желтым; из этого раствора вода
осаждает гидрат Mn(OH) 4, a MnSO4
— двойную соль Mn(SO 4)2.MnSO4.9Н 2 O,
в виде шестиугольных табличек, растворимых в слабой серной кислоте с красным
цветом. С давних пор, как выше упомянуто, пиролюзит употребляется при
выделке стекла, именно для уничтожения зеленого цвета, что, вероятно, происходит
вследствие окисляющего действия MnО 2
на закись железа, а потому этот минерал получил название "мыла стеклоделов",
действующего на огне (πυρ — огонь, λύω — мою). Очень важное значение пиролюзит
имеет для добычи хлора, потому что уже при слабом нагревании с соляной кислотой
или с поваренной солью и разведенной серной кислотой идет реакция ,
с кислотами они не дают перекиси
водорода, хотя последняя в присутствии аммиака и осаждает из раствора МnХ 2
двуокись; состав осадка Mn 6O11=5MnO2 MnO
(A. Carnot)], подобно РbО 2,
обладает слабыми кислотными свойствами, а потому образует с основаниями
солеподобные соединения, манганиты. Важнейшая руда. М., пиролюзит, есть почти
чистая двуокись, встречается в виде квадратных кристаллов и в виде масс,
кристаллического характера; обладает стально-серым или черным цветом и
металлическим блеском, уд. в. 4,82. Из солеподобных соединений в природе
находятся псиломелан — (Мn, Ва)О.2МnО 2,
манганит Мn 2O2 (ОН) 2,
который можно представить чрез МnО. МnО 2.H2 O
[В природе встречается обыкновенно
вместе с известковым и тяжелым
шпатом]. Искусственно МnО 2
можно получить, если промыть азотной кислотой, при кипячении, остаток после
слабого каления Mn(NO 3)2
или MnСО 3 при
доступе воздуха; в первом случае промывается черная окись Mn 2O3,
во втором — красная закись-окись Mn 3O4
(см. ниже); так как в обоих случаях остается до промывании двуокись, то и Mn 2O3,
и Mn 3O4
должно считать солеподоб.
веществами, как Pb 2O3
и Pb 3O4
(сурик), которые точно так же при действии HNO 3
дают PbO 2.
Двуокись М. можно получить и в виде гидрата, если действовать на раствор MnХ 2
раствором хлора или брома в едкой щелочи или если промыть гидрат Mn 2O3
азотной кислотой; такой гидрат MnО 2,
промытый водой, растворим с бурым цветом (Gorgen); раствор обладает кислой
реакцией, сохраняется в течение недель; малые количества щелочей или кислот
осаждают гидрат (свертывают) [Получены след. калиевые соли этой кислоты: K 2O.5MnO2
— желтый осадок, образующийся
при действии углекислоты на раствор K 2MnO4; K2O.MnO2
— темно-бурый порошок,
получается при нагревании KMnО 4,
второй манганит водой разлагается на КОН и первый манганит]. Но двуокись М.
обладает и свойствами основными; если действовать при охлаждении на MnO 2,
разболтанную в эфире, хлористым водородом, то получается зеленый раствор, по
всей вероятности MnCl 4
(аналогично действуют и НВк и HJ); при -26° MnCl 4
почти не разлагается в водном растворе (Vernon, 1892); с крепкой плавиковой
кислотой получается из MnО 2
несомненно MnF 4,
потому что бурый раствор, получающийся при этом с KF, дает розовый осадок
состава K 2MnF6.
Если смешать 1 часть марганцево-кислого калия (см. ниже) с 5 ч. Н 2 SО 4
и 1 1/2
ч. H 2 O, то по
мере выделения кислорода раствор делается желтым; из этого раствора вода
осаждает гидрат Mn(OH) 4, a MnSO4
— двойную соль Mn(SO 4)2.MnSO4.9Н 2 O,
в виде шестиугольных табличек, растворимых в слабой серной кислоте с красным
цветом. С давних пор, как выше упомянуто, пиролюзит употребляется при
выделке стекла, именно для уничтожения зеленого цвета, что, вероятно, происходит
вследствие окисляющего действия MnО 2
на закись железа, а потому этот минерал получил название "мыла стеклоделов",
действующего на огне (πυρ — огонь, λύω — мою). Очень важное значение пиролюзит
имеет для добычи хлора, потому что уже при слабом нагревании с соляной кислотой
или с поваренной солью и разведенной серной кислотой идет реакция
MnО 2 + 4НСl =
MnСl 2 + 2Н 2 O
+ Сl 2.
Довольно давно возникла мысль превращать MnО, находящуюся в остатках после
добывания хлора, опять в MnO 2.
С 1867 г. часто применяется следующий путь (Walter Weldon): кислая жидкость
нейтрализуется углекислой известью, при чем осаждается окись железа; прозрачный
раствор смешивают с известковым молоком, нагревают паром и вдувают сильную струю
воздуха; в этих условиях, вероятно, благодаря присутствии извести, MnО
окисляется до MnО 2,
которая и получается затем в осадке и может быть снова пущена в дело.
Окись М.,
Mn2O3, и соли
типа MnХ 3. Выше
указано, что окисел этого типа с азотной кислотой дает MnO 2:
последняя извлекает из него MnО. Но Mn 2O3
имеет и самостоятельное значение, подобно Аl 2O3, Fe2O3.
В природе Mn 2O3
представляет минерал браунит (см.); искусственно получается при
накаливании всякого другого окисла М. в струе кислорода или смеси его с азотом,
но содержащей более 26% кислорода, в виде черного порошка, уд. веса 4,32.
Соответственные соли MnCl 3
и Mn 2(SO4)3
известны только в растворах и легко разлагаются с выделением Cl или О, но
двойные соли сравнительно прочны: например квасцы K 2Mn2(SO4)4.24Н 2 O,
которые образуют фиолетовые октаэдры, фиолетово-красные кристаллы (NH 4)2MnCl5
и К 2 MnСl 5
(Neumann), а также вышеупомянутая двойная соль, аналогичная красной соли
Гмелина, К 3 MnСу 6.
Квасцы водой разлагаются с образованием гидрата окиси Mn 2O2 (ОН) 2.
Этот гидрат встречается, как упомянуто, и в природе под именем манганита,
в виде стально-серых или черных квадратных кристаллов, уд. веса 4,3; он очень
похож на пиролюзит, но черта, проведенная на неглазурованном фарфоре от
пиролюзита — черная, а от манганита — бурая.
Закись-окись М.
Mn3O4, или
красная окись, встречается в бурых ромбических пирамидах под названием
гаусманнита, уд. вес которого 4,85. Этот окисел получается при прокаливании
на воздухе всех окислов М. в виде красно-бурого порошка, уд. веса 4,72; она
превращается в кристаллы гаусманнита при нагревании в слабом токе НСl. В
холодной крепкой серной кислоте Mn 3O4
растворяется с красным цветом, превращаясь в Mn 2(SO4)3
и MnSO 4, а при
нагревании с разведенной серной кислотой дает 2MnSO 4
и MnО 2, так же и
при действии кипящей азотной кислоты (см. выше).
Марганцовистый и марганцевый ангидриды, MnО 3
и Mn 2O7.
Глаубер (1659) уже сообщает, что при сплавлении пиролюзита с едкой щелочью
получается масса, растворяющаяся в воде с пурпуровым цветом, который
превращается затем в зеленый. В сочинении неизвестного автора "Ключ к тайному
кабинету сокровищницы природы" (1705) говорится о подобном же сплаве, который
растворяется, однако, с серо-зеленым цветом; цвет раствора делается затем
небесно-голубым, фиолетовым и наконец красным. Шееле дал продукту сплавления
название "минерального хамелеона". Сущность дела уяснена Э. Митчерлихом. Не
только двуокись, но и низшие окислы при сплавлении со щелочью дают зеленый
продукт, при чем совершается поглощение кислорода из воздуха; прибавление
селитры способствует превращению; здесь образуется зеленая соль состава К 2 MnО 4;
раствор ее при избытке щелочи постоянен и обладает тем же цветом. Если
нейтрализовать часть щелочи кислотой, то цвет раствора меняется в фиолетовый и
красный, вследствие превращения в др. соль
3К 2 MnО 4
+ 2Н 2 O = 2КMnО 4
+ 4КОН + MnО 2;
это превращение совершается и при содействии углекислоты, и при простом
разбавлении водой, при чем раствор мутится, вследствие осаждения двуокиси. КMnО 4
есть марганцево-, а К 2 MnО 4
марганцовисто-кислый калий.
Если кипятить КMnО 4
в крепком щелочном растворе, то идет обратное превращение при выделении
кислорода
4КMnО 4 + 4КOH
= 4K 2 MnО 4
+ 2Н 2 O + О 2;
прибавление веществ, способных окисляться (напр. спирта), способствует
превращению; так же действует и органического происхождения пыль, попадая из
воздуха в щелочной раствор КMnО 4. Na2MnO4.10H2 О
походит на глауберову соль, а ВаMnО 4
не растворим в воде (подобно BaSO 4)
и кислотами разлагается. Соответственная кислота Н 2 MnО 4
неизвестна, а ангидрид MnО 3
представляет собой (Thorpe) аморфную расплывчатую красноватую массу, кажущуюся в
отраженном свете почти черной. Если к хорошо охлажденной крепкой серной кислоте
прибавлять постепенно KMnO 4,
то получается зеленый раствор, а на
дне собирается темно-красно-бурая жидкость, не застывающая при -20° и очень
непостоянная; это марганцевый ангидрид MnO 7,
при нагревании взрывающий [При чем появляется даже огонь; то же происходит при
соприкосновении с бумагой и другими органическими веществами или если бросить
одну каплю в сосуд, содержащий пары спирта, эфира, сероводорода и проч.] и
растворяющийся в воде с разогреванием; получающийся при этом красный раствор
содержит кислоту НMnО 4.
Упомянутый зеленый сернокислый раствор, образующийся над слоем Mn 2O7,
содержит, вероятно, вещество состава (Mn 2O6)SO4.
Если к такому раствору прибавлять осторожно, при охлаждении, плавленой
поваренной соли, то выделяется марганцевый хлорангидрид MnO 3 Cl
(Ascboff), по уравн.:
(Mn2O6)SO4 + 2NaCl = Na2SO4
+ 2MnO З Cl
в виде желтого газа, сгущающегося в охладительной смеси в зеленовато-бурую
жидкость, обладающую свойствами хлорангидридов и взрывающую при нагревании. Из
того же зеленого раствора был получен (Thorpe) марганцовистый ангидрид;
при медленном прибавлении раствора к безводной соде по ур.:
(Mn2O6)SO4 + Na2CO3 =
MnO3 + Na2SO4 + CO2 + O
ангидрид в виде порошка уносился током газов (СО 2
и О) и собирался в трубке, наполненной битым стеклом. Обыкновенный препарат из
этой группы соединений есть KMnO 4,
который часто называют "хамелеоном". В совершенно чистом виде он может быть
получен (Грегори) так: возможно крепкий раствор 10 ч. КОН смешивают с 7 ч. КСlО 3
и 8 ч. MnО 2,
выпаривают досуха и остаток нагревают при темно-красном калении до полного
разложения КСlО 3;
темно-зеленая масса извлекается водой; отстоявшийся раствор фильтруется через
асбест и подвергается кристаллизации; выделяются длинные призмы КMnО 4,
изоморфные с КСlО 4.
Хамелеон растворим в 15 частях холодной воды; раствор обладает густым пурпуровым
цветом. В химической практике хамелеон является окислителем; окисления
совершаются особенно легко в присутствии избытка разведенной серной кислоты.
Смесь хамелеона с серой взрывает при ударе, смесь с порошкообразным магнием
горит очень быстро (см.
Магний); раствор КMnО 4
употребляется при очищении водорода (для окисления AsH 3
и пр. примесей), как реактив для окисления органических соединений (Е. Е.
Вагнер). В присутствии серной кислоты окислителем является, очевидно, свободная
кислота НMnО 4.
Относительно применения окислительной способности хамелеона в объемном анализе
см. в ст. Железо (анализ), Окислы азота, Оксидиметрия. Хамелеон употребляется
при определении азота в органических соединениях, по Кьельдалю, для того, чтобы
закончить окисление органического вещества, начатое крепкой серной кислотой;
азот здесь при избытке кислоты получается в виде серноаммиачной соли; свободный
аммиак хамелеоном окисляется. Фабричное производство солей марганцевой и
марганцовистой кислот развилось со времени применения их для дезинфекции
(Hofmann, 1859), для чего готовят менее чистые натриевые препараты.
Из других соединений М. должно упомянуть о соединениях с серой и азотом.
Сернистый M., MnS, находится в природе в виде марганцевого блеска,
стально-серой массы или кристаллов (кубов), уд. в. 4,04; искусственно получают
при накаливании в токе H 2 S
закиси или ее солей; из растворов MnХ 2
сернистый аммоний осаждает
тельно-розовый осадок, буреющий на воздухе, при нагревании под раствором
превращающийся в зеленый гидрат 3MnS.Н 2 O.
Минерал гауэрит, MnS2,
большие буро-черные октаэдры; отвечает по составу двуокиси; при нагревании MnSO 4
с раствором многосернистого калия при 160-180° в запаянной трубке получается
кирпично-красный порошок того же состава. Два соединения с азотом,
Mn5N2 и Mn 3N2
получены недавно (О. Prelinger) и представляют твердые вещества уд. веса 6,58 и
6,21, обладающие металлическим блеском; первое получается при накаливании в
струе азота, а второе в струе аммиака — металлического М. из электролизом
полученной амальгамы; можно и не выделять предварительно металл из амальгамы, а
прямо ею пользоваться. Если нагревать в струе азота амальгаму, то, когда отгонка
ртути оканчивается, замечается значительное разогревание трубки, в которой
производится операция. M n3N2
при прокаливании в струе азота превращается в Mn 5N2
, а это соединение в струе аммиака
дает вновь Mn 3N2. Mn5N2
при нагревании в струе водорода дает аммиак, а также и при действии щелочей и
даже воды; химические отношения Mn 3N2
таковы же.
При систематическом анализе соляных смесей, М., по осаждении
углекислым барием гидратов окисей типа R 2O3,
оказывается в растворе вместе с цинком; по осаждении сернистым аммонием его
извлекают из осадка уксусной кислотой, которая не растворяет ZnS; из раствора,
не содержащего других металлов, М. осаждают содой и взвешивают в виде Mn 3O4.
При сокращенных способах отделения М. оказывается нередко с магнием, подобно
которому он трудно осаждается в присутствии аммиачных солей; отделение в таких
случаях основывается на переводе MnХ 2
в MnO 2, действием
галоида в щелочном растворе. Техническое испытание марганцевых руд и препаратов
нередко сводится к определению в них кислорода, способного выделять хлор с
соляной кислотой; отвешенное количество испытуемого материала обрабатывают
соляной кислотой, улавливают хлор раствором KJ и определяют йод, сделавшийся
свободным (см. Йодометрия).
С. С. Колотов, Δ .
|