Большая Советская
Энциклопедия
|
|
|
|
источник статьи: Большая Советская Энциклопедия |
|
Гелий (лат. Helium), символ Не, химический элемент VIII группы периодической системы, относится к инертным газам; порядковый номер 2, атомная масса 4,0026; газ без цвета и запаха. Природный Г. состоит из 2 стабильных изотопов: 3He и 4He (содержание 4He резко преобладает). Впервые Г. был открыт не на Земле, где его мало, а в атмосфере Солнца. В 1868 француз Ж. Жансен и англичанин Дж. Н. Локьер исследовали спектроскопически состав солнечных протуберанцев. Полученные ими снимки содержали яркую жёлтую линию (т. н. D3-линию), которую нельзя было приписать ни одному из известных в то время элементов. В 1871 Локьер объяснил её происхождение присутствием на Солнце нового элемента, который и назвали гелием (от греч. helios — Солнце). На Земле Г. впервые был выделен в 1895 англичанином У. Рамзаем из радиоактивного минерала клевеита. В спектре газа, выделенного при нагревании клевеита, оказалась та же линия. Гелий в природе. На Земле Г. мало: 1 м3 воздуха содержит всего 5,24 см3 Г., а каждый килограмм земного материала — 0,003 мг Г. По распространённости же во Вселенной Г. занимает 2-е место после водорода: на долю Г. приходится около 23% космической массы. На Земле Г. (точнее, изотоп 4He) постоянно образуется при распаде урана, тория и других радиоактивных элементов (всего в земной коре содержится около 29 радиоактивных изотопов, продуцирующих 4He). Примерно половина всего Г. сосредоточена в земной коре, главным образом в её гранитной оболочке, аккумулировавшей основные запасы радиоактивных элементов. Содержание Г. в земной коре невелико — 3 · 10-7% по массе. Г. накапливается в свободных газовых скоплениях недр и в нефтях; такие месторождения достигают промышленных масштабов. Максимальные концентрации Г. (10—13%) выявлены в свободных газовых скоплениях и газах ура новых рудников и (20—25%) в газах, спонтанно выделяющихся из подземных вод. Чем древнее возраст газоносных осадочных пород и чем выше в них содержание радиоактивных элементов, тем больше Г. в составе природных газов. Вулканическим газам свойственно обычно низкое содержание Г. Добыча Г. в промышленных масштабах производится из природных и нефтяных газов как углеводородного, так и азотного состава. По качеству сырья гелиевые месторождения подразделяются: на богатые (содержание Не > 0,5% по объёму); рядовые (0,10—0,50) и бедные < 0,10). В СССР природный Г. содержится во многих нефтегазовых месторождениях. Значительные его концентрации известны в некоторых месторождениях природного газа Канады, США (шт. Канзас, Техас, Нью-Мексико, Юта). В природном Г. любого происхождения (атмосферном, из природных газов, из радиоактивных минералов, метеоритном и т.д.) преобладает изотоп 4He. Содержание 3He обычно мало (в зависимости от источника Г. оно колеблется от 1,3 · 10-4 до 2 · 10-8%) и только в Г., выделенном из метеоритов, достигает 17—31,5%. Скорость образования 4He при радиоактивном распаде невелика: в 1 т гранита, содержащего, например, 3 г урана и 15 г тория, образуется 1 мг Г. за 7,9 млн. лет; однако, поскольку этот процесс протекает постоянно, за время существования Земли он должен был бы обеспечить содержание Г. в атмосфере, литосфере и гидросфере, значительно превышающее наличное (оно составляет около 5 · 1014 м3). Такой дефицит Г. объясняется постоянным улетучиванием его из атмосферы. Лёгкие атомы Г., попадая в верхние слои атмосферы, постепенно приобретают там скорость выше 2-й космической и тем самым получают возможность преодолеть силы земного притяжения. Одновременное образование и улетучивание Г. приводят к тому, что концентрация его в атмосфере практически постоянна. Изотоп 3He, в частности, образуется в атмосфере при бета-распаде тяжёлого изотопа < u>водорода — трития (Т), возникающего, в свою очередь, при взаимодействии нейтронов космического излучения с азотом воздуха: Ядра атома 4He (состоящие из 2 протонов и 2 нейтронов), называют альфа-частицами или гелионами, — самые устойчивые среди составных ядер. Энергия связи нуклонов (протонов и нейтронов) в 4He имеет максимальное по сравнению с ядрами других элементов значение (28,2937 Мэв); поэтому образование ядер 4He из ядер водорода (протонов) 1Н сопровождается выделением огромного количества энергии. Считают, что эта ядерная реакция: 41H = 4He +2b+ + 2n [одновременно с 4He образуются 2 позитрона (b +) и 2 нейтрино (n)] служит основным источником энергии Солнца и других схожих с ним звёзд. Благодаря этому процессу и накапливаются весьма значительные запасы Г. во Вселенной. Физические и химические свойства. При нормальных условиях Г. — одноатомный газ без цвета и запаха. Плотность 0,17846 г/л, tkип — 268,93°С. Г. — единственный элемент, который в жидком состоянии не отвердевает при нормальном давлении, как бы глубоко его ни охлаждали. Наименьшее давление перехода жидкого Г. в твёрдый 2,5 Мн/м2 (25 am), tпл при этом равна — 272,1°С. Теплопроводность (при 0°С) 143,8 · 10-3 вт/см (K [343,4 · 10-6 кал/(см (град (сек)]. Радиус атома Г., определённый различными методами, составляет от 0,85 до 1,33 До настоящего времени попытки получить устойчивые химические соединения Г. оканчивались неудачами (см. Инертные газы). Спектроскопически доказано существование в разряде иона He2+. В 1967 советские исследователи В. П. Бочин, Н. В. Закурин, В. К. Капышев сообщили о синтезе в зоне дугового разряда за счёт реакции Г. с фтором, с BF3 или с RuF5 ионов HeF+, HeF22+ и HeF2+. Согласно расчёту, величина энергии диссоциации иона HeF+ равна 2,2 эв. Получение и применение. В промышленности Г. получают из гелийсодержащих природных газов (в настоящее время эксплуатируются гл авным образом месторождения, содержащие > 0,1% Г.). От других газов Г. отделяют методом глубокого охлаждения, используя то, что он сжижается труднее всех остальных газов. Благодаря инертности Г. широко применяют для создания защитной атмосферы при плавке, резке и сварке активных металлов. Г. менее электропроводен, чем другой инертный газ — аргон, и поэтому электрическая дуга в атмосфере Г. даёт более высокие температуры, что значительно повышает скорость дуговой сварки. Благодаря небольшой плотности в сочетании с негорючестью Г. применяют для наполнения стратостатов. Высокая теплопроводность Г., его химическая инертность и крайне малая способность вступать в ядерную реакцию с нейтронами позволяют использовать Г. для охлаждения атомных реакторов. Жидкий Г. — самая холодная жидкость на Земле, служит хладагентом при проведении различных научных исследований. На определении содержания Г. в радиоактивных минералах основан один из методов определения их абсолютного возраста (см. Геохронология). Благодаря тому что Г. очень плохо растворим в крови, его используют как составную часть искусственного воздуха, подаваемого для дыхания водолазам (замена азота на Г. предотвращает появление кессонной болезни). Изучаются возможности применения Г. и в атмосфере кабины космического корабля. С. С. Бердоносов, В. П. Якуцени. Гелий жидкий. Относительно слабое взаимодействие атомов Г. приводит к тому, что он остаётся газообразным до более низких температур, чем любой другой газ. Максимальная температура, ниже которой он может быть сжижен (его критическая температура TK), равна 5,20 К. Жидкий Г. — единственная незамерзающая жидкость: при нормальном давлении (рис. 1) Г. остаётся жидким при сколь угодно низких температурах и затвердевает лишь при давлениях, превышающих 2,5 Мн/м2 (25 am). При температуре T В 1938 П. Л. Капица открыл у Не II сверхтекучесть — способность течь практически без вязкости. Объяснение этого явления было дано Л. Д. Ландау (1941) на основе квантовомеханических представлений о характере теплового движения в жидком Г. При низких температурах это движение описывается как сущес твование в жидком Г. элементарных возбуждений — фононов (квантов звука), обладающих энергией e·= hv (v — частота звука, h — постоянная Планка) и импульсом р = e/c (с = 240 м/сек — скорость звука). Число и энергия фононов растут с повышением температуры Т. При T > 0,6 К появляются возбуждения с большими энергиями (ротоны), для которых зависимость e(p) имеет нелинейный характер. Фононы и ротоны (см. Квазичастицы) обладают импульсом и, следовательно, массой. Отнесённая к 1 см, эта масса определяет плотность rn т. н. нормальной компоненты жидкого Г. При низких температурах rn< /i> стремится к нулю при Т ® 0. Движение нормальной компоненты, как и обычного газа, имеет вязкостный характер. Остальная часть жидкого Г., т. н. сверхтекучая компонента, движется без трения; её плотность rs = r — rn. При Т ® Tl rn ® r, так что в l-точке rs обращается в нуль и сверхтекучесть исчезает (Не I — обычная вязкая жидкость). Т. о., в жидком Г. одновременно могут происходить два движения с различными скоростями. На основе этих представлений удаётся о бъяснить ряд наблюдаемых эффектов: при вытекании He II из сосуда через узкий капилляр температура в сосуде повышается, т.к. вытекает главным образом сверхтекучая компонента, не несущая с собой теплоты (т. н. механокалорический эффект); при создании разности температур между концами закрытого капилляра с Не II в нём возникает движение (термомеханический эффект) — сверхтекучая компонента движется от холодного конца к горячему и там превращается в нормальную, которая движется навстречу, при этом суммарный поток отсутствует. В жидком Г. может распространяться звук двух видов — обычный и т. н. второй звук. При распространении второго звука в местах сгущения нормальной компоненты происходит разрежение сверхтекучей. Всё сказанное относится к обычному Г., состоящему в основном из изотопа 4He. Более редкий изотоп 3He имеет иные, чем у 4He, квантовые свойства (см. Квантовая жидкость). Жидкий 3He — также незамерзающая жидкость (TK = 3,33 К), но не обладающая сверхтекучестью: вязкость 3He неограниченно возрастает с понижением температуры. Л. П. Питаевский.
Лит.: Кеезом В., Гелий, пер. с англ., М., 1949; Фастовский В. Г., Ровинский А. Е., Петровский Ю. В., Инертные газы, М., 1964; Халатников И. М., Введение в теорию сверхтекучести, М., 1965; Смирнов Ю. Н., Гелий вблизи абсолютного нуля, «Природа», 1967, № 10, с. 70; Якуцени В. П., Геология гелия, Л., 1968. См. также лит. к ст. Инертные газы.
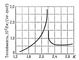 Рис. 2. Теплоёмкость жидкого 4He вблизи l-точки. Кривая имеет характерную форму, нап оминающую греческую букву l.  Рис. 1. Диаграмма состояния 4He.  Рис. 3. Плотность r жидкого 4He вблизи l-точки. |